题目内容
1.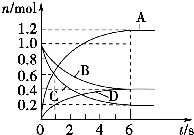 一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )| A. | 该反应的化学方程式为3B+4C?6A+2D | |
| B. | 反应进行到1 s时,v(A)和v(D)不相等 | |
| C. | 反应进行到6 s时,B的平均反应速率为0.05 mol•L-1•s-1 | |
| D. | 反应进行到6 s时,各物质的浓度不再变化,反应速率为零 |
分析 A、根据图象中的有关数据判断四种物质的变化,再根据计量数之比等于物质的量的变化量之比;
B、根据v=$\frac{△c}{△t}$,可判断;
C、根据v=$\frac{△c}{△t}$进行计算;
D、根据图象判断反应平衡状态,再据此判断;
解答 解:A、由图可知,反应达到平衡时A物质增加了1.2mol、D物质增加了0.4mol、B物质减少了0.6mol、C物质了0.8mol,所以A、D为生成物,物质的量之比为3:1,B、C为反应物,物质的量之比为3:4,反应方程式为:3B+4C?6A+2D,故A正确;
B、反应到1s时,v(A)=$\frac{△c}{△t}$=$\frac{\frac{0.6mol}{2L}}{1s}$=0.3mol/(L•s),v(D)=$\frac{△c}{△t}$=$\frac{\frac{0.2mol}{2L}}{1s}$=0.1mol/(L•s),所以v(A)≠v(D),故B正确;
C、反应进行到6s时,v(B)=$\frac{△c}{△t}$=$\frac{\frac{0.6mol}{2L}}{6s}$=0.05mol/(L•s),故C正确;
D、根据图象可知,到6s时各物质的物质的量不再改变了,达到平衡状态,各物质的浓度不再变化,正逆反应速率相同反应速率不为零,故D错误;
故选D.
点评 本题主要考查了可逆反应的书写、化学平衡的特征、及化学反应的计算,本题解题的关键是根据图象找出相关信息,对学生的识图能力有一定的要求,中等难度.

练习册系列答案
相关题目
11.用已知物质的量浓度的盐酸滴定未知物质的量浓度的氢氧化钠溶液,下列操作会导致测定结果偏高的是( )
| A. | 用标准的盐酸溶液润洗酸式滴定管2-3次 | |
| B. | 用待测碱液润洗碱式滴定管2-3次 | |
| C. | 用待测碱液润洗锥形瓶2-3次 | |
| D. | 用蒸馏水润洗锥形瓶2-3次 |
12.下列实验操作:①用50mL量筒量取5mL蒸馏水;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要立即用大量水冲洗;④倾倒液体时试剂不对准容器口;⑤块状药品都要用药匙取用;⑥固体药品用细口瓶保存.其中错误的是( )
| A. | ①②③ | B. | ③④ | C. | ②⑤⑥ | D. | ①②③④⑤⑥ |
9.氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应,用CuSO4溶液和“某物质”在40-50℃时反应可产生它.下列有关叙述中错误的是( )
| A. | 这“某物质”具有还原性 | |
| B. | CuH与盐酸反应,可能产生H2 | |
| C. | CuH与足量的稀硝酸反应:CuH+3H++NO3-=Cu2++NO↑+2H2O | |
| D. | CuH在氯气中燃烧:CuH+Cl2=CuCl+HCl |
6.下列离子方程式表达正确的是( )
| A. | 少量小苏打溶液和澄清石灰水反应:HCO${\;}_{3}^{-}$+OH-+Ca2+═CaCO3↓+H2O | |
| B. | 氢氧化钡溶液跟硫酸反应:Ba2++SO${\;}_{4}^{2-}$+OH-+H+═BaSO4↑+H2O | |
| C. | 三氯化铁溶液跟氨水反应:Fe3++3OH-═Fe(OH)3↓ | |
| D. | 实验室制二氧化碳:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O |
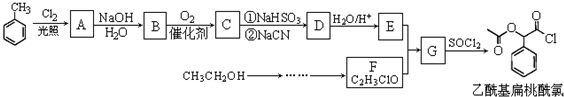

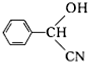 .
.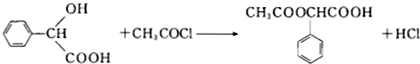 .
. .
.