��Ŀ����
11��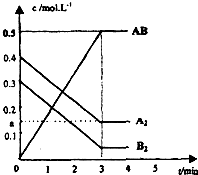 ��һ���ݻ�Ϊ2L���ܱ������У�����0.8mol��A2�����0.6molB2���壬һ�������·������·�Ӧ��A2��g��+B2��g��?2AB��g����H��0����Ӧ�и����ʵ�Ũ����ʱ��ı仯�����ͼ��ʾ��
��һ���ݻ�Ϊ2L���ܱ������У�����0.8mol��A2�����0.6molB2���壬һ�������·������·�Ӧ��A2��g��+B2��g��?2AB��g����H��0����Ӧ�и����ʵ�Ũ����ʱ��ı仯�����ͼ��ʾ����1����������Ӧ�ﵽƽ���4minʱ�����������������������һ���������������䣩������ͼ�л���4min��5min��ABŨ�ȵı仯�ߣ�
��2������ͬ�����£�����ʼʱ��������м����A2��g����B2��g����AB��g�������ʵ����ֱ�Ϊ0.4mol��0.2mol��0.8mol����Ӧ������Ӧ������У���������桱�����ж�������Ũ����Qc=$\frac{0��{4}^{2}}{0.2��0.1}$=8��K=$\frac{0��{5}^{2}}{0.15��0.05}$=$\frac{100}{3}$����Ӧ������Ӧ���У���Ӧ�ﵽƽ������ʵ����������ԭƽ����Ȣۣ�����ţ�
��A2��B2��С��AB���� ��A2��B2����AB��С �۾����� ����ȷ����
���� ��1��������Ӧ�ﵽƽ���4minʱ�����������������������һ����˲��AB��Ũ�ȱ�Ϊԭ����һ�룬�÷�Ӧ��Ӧǰ������������䣬ѹǿֻ�ı䷴Ӧ���ʣ����ı�ƽ���ƶ���
��2������ͼ��֪��ƽ��ʱAB��Ũ�ȱ仯Ϊ0.5mol/L����A2��Ũ�ȱ仯Ϊ0.25mol/L������a=0.4mol/L-0.25mol/L=0.15mol/L��ƽ��ʱB2��Ũ��Ϊ0.3mol/L-0.25mol/L=0.05mol/L������K=$\frac{{c}^{2}��AB��}{c��{A}_{2}����c��{B}_{2}��}$����ƽ�ⳣ���������ʱŨ����Qc����Qc=K������ƽ��״̬����Qc��K����Ӧ������Ӧ���У���Qc��K����Ӧ���淴Ӧ���У�
����ʼʱ��������м����A2��g����B2��g����AB��g�������ʵ����ֱ�Ϊ0.4mol��0.2mol��0.8mol����ЧΪ��ʼ�������0.8mol��A2�����0.6molB2���壬��ԭƽ��Ϊ��ȫ��Чƽ�⣬ƽ��ʱ��ͬ��ֵ����ʵ���Ũ����ȣ�
��� �⣺��1��������Ӧ�ﵽƽ���4minʱ�����������������������һ����˲��AB��Ũ�ȱ�Ϊԭ����һ�룬�÷�Ӧ��Ӧǰ������������䣬ѹǿֻ�ı䷴Ӧ���ʣ����ı�ƽ���ƶ���4min��5min��ABŨ�ȵı仯��Ϊ��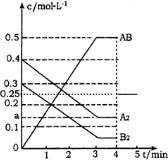 ��
��
�ʴ�Ϊ�� ��
��
��2������ͼ��֪��ƽ��ʱAB��Ũ�ȱ仯Ϊ0.5mol/L����A2��Ũ�ȱ仯Ϊ0.25mol/L������a=0.4mol/L-0.25mol/L=0.15mol/L��ƽ��ʱB2��Ũ��Ϊ0.3mol/L-0.25mol/L=0.05mol/L��ƽ�ⳣ��K=$\frac{{c}^{2}��AB��}{c��{A}_{2}����c��{B}_{2}��}$=$\frac{0��{5}^{2}}{0.15��0.05}$=$\frac{100}{3}$��
����ʼʱ��������м����A2��g����B2��g����AB��g�������ʵ����ֱ�Ϊ0.4mol��0.2mol��0.8mol��Ũ����Qc=$\frac{0��{4}^{2}}{0.2��0.1}$=8��K=$\frac{0��{5}^{2}}{0.15��0.05}$=$\frac{100}{3}$����Ӧ������Ӧ���У�
����ʼʱ��������м����A2��g����B2��g����AB��g�������ʵ����ֱ�Ϊ0.4mol��0.2mol��0.8mol����ЧΪ��ʼ�������0.8mol��A2�����0.6molB2���壬���º����£���ԭƽ��Ϊ��ȫ��Чƽ�⣬ƽ��ʱ��ͬ��ֵ����ʵ���Ũ����ȣ���Ӧ�ﵽƽ������ʵ����������ԭƽ����Ⱦ����䣬
�ʴ�Ϊ������Ӧ��Ũ����Qc=$\frac{0��{4}^{2}}{0.2��0.1}$=8��K=$\frac{0��{5}^{2}}{0.15��0.05}$=$\frac{100}{3}$����Ӧ������Ӧ���У��ۣ�
���� ���⿼�黯ѧƽ����йؼ��㡢ƽ�ⳣ��Ӧ�á���Чƽ��ȣ��Ѷ��еȣ���2����ע��Ե�Чƽ����ɵ����⣮

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| ��� | �Լ� | ���淽�� | ���� |
| A | �� | �����ʢ��ú�͵�ϸ��ƿ�� | ��ֹ��O2��H2O��Ӧ |
| B | ̼���ƾ��� | ����ڸ����ܱյĹ��ƿ�� | ��ֹ�绯������ |
| C | ������ˮ | ����ڴ���Ƥ����ϸ��ƿ�� | ��ֹ�ӷ�����ֹƿ����ƿ��ճ�� |
| D | ������������ | ����ڴ���Ƥ���Ĺ��ƿ�� | ��ֹ�Ӵ���������������ֹ��ˮ������������̼�Ӵ������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | 0.05 mol | B�� | 1 mol | C�� | 0.1 mol | D�� | 0.2 mol |
| A�� | δ��ȴ��ת�ơ����� | B�� | δϴ���ձ��������� | ||
| C�� | ����ʱ���ӿ̶��߹۲�Һ�� | D�� | ����ƿԭ����������ˮ |
| A�� | 1��2��3 | B�� | 1��3��3 | C�� | 1��6��9 | D�� | 1��3��6 |
| A�� | �����������������������Һ��Ӧ��Fe��OH��3+3H+=Fe3++3H2O | |
| B�� | ����������Һ�м������������Һ��2Fe2++H2O2+2H+=2Fe3++2H2O | |
| C�� | NaHCO3��Һ�м�������ʯ��ˮ��HCO3-+Ca2++OH-=CaCO3��+H2O | |
| D�� | ��NaAlO2��Һ��ͨ������CO2��2AlO2-+CO2+3H2O�T2Al��OH��3��+CO32- |