题目内容
3.32g铜跟适量的浓硝酸反应,铜全部作用后,共收集到NO、NO2混合气体22.4L(标准状况下),则反应消耗的硝酸的物质的量是( )| A. | 1.0 mol | B. | 1.5 mol | C. | 2.0 mol | D. | 2.5 mol |
分析 根据混合气体的物质的量可得被还原的硝酸的物质的量,根据生成硝酸铜的物质的量可知表现酸性的硝酸的物质的量,以此计算反应消耗的硝酸的物质的量.
解答 解:铜和硝酸反应,随着浓度的减少,硝酸的还原产物的价态越低,铜和浓硝酸反应生成NO2,而与稀硝酸反应时则生成NO,故生成的气体有NO2和NO,
则n(NO2)+n(NO)=$\frac{22.4L}{22.4L/mol}$=1mol,即被还原的硝酸的物质的量为1mol,
n(Cu)=$\frac{32}{64g/mol}$=0.5mol,则生成n(Cu(NO3)2)=0.5mol,
可知表现酸性的硝酸的物质的量为0.5mol×2=1mol,
则参加反应的硝酸的物质的量为1mol+1mol=2mol.
故选C.
点评 本题以硝酸为载体考查了物质的量的计算,根据硝酸铜的化学式及N原子守恒计算消耗硝酸的物质的量,题目难度不大.

练习册系列答案
相关题目
13.为验证氧化性Cl2>Fe3+>SO2,某小组用如图1所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验).
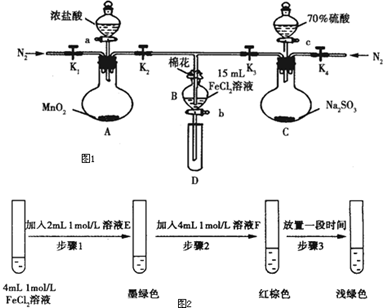
实验过程:
Ⅰ.打开弹簧夹K1~K4,通过一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K2、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K2,活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K2.
Ⅵ.更换试管D,重复过程Ⅳ,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰实验.
(2)棉花中浸润的溶液为NaOH溶液.
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是70%硫酸中氢离子浓度大于98%的硫酸,因此反应速率更快.
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是乙、丙(填“甲”、“乙”或“丙”).
(6)进行实验过程Ⅴ时,B中溶液颜色由黄色逐渐变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色.
查阅资料:Fe2+(aq)+2SO32-(aq)?FeSO3(s)(墨绿色)
提出假设:FeCl2与SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色.
某同学设计如图2实验,证实该假设成立:
①溶液E和F分别为Na2SO3、FeCl3.
②请用离子方程式解释步骤3中溶液(酸性)由红棕色变浅绿色的原因Fe3+消耗SO32-,c(SO32-)减小,平衡Fe2+(aq)+SO32-(aq)?FeSO3(s)(墨绿色)逆向移动,溶液颜色由红棕色变为浅绿色.

实验过程:
Ⅰ.打开弹簧夹K1~K4,通过一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K2、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K2,活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K2.
Ⅵ.更换试管D,重复过程Ⅳ,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰实验.
(2)棉花中浸润的溶液为NaOH溶液.
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是70%硫酸中氢离子浓度大于98%的硫酸,因此反应速率更快.
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是乙、丙(填“甲”、“乙”或“丙”).
| 过程Ⅳ:B溶液中含有的离子 | 过程Ⅵ:B溶液中含有的离子 | |
| 甲 | 有Fe3+,无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+、又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+、无Fe2+ | 有Fe2+ |
查阅资料:Fe2+(aq)+2SO32-(aq)?FeSO3(s)(墨绿色)
提出假设:FeCl2与SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色.
某同学设计如图2实验,证实该假设成立:
①溶液E和F分别为Na2SO3、FeCl3.
②请用离子方程式解释步骤3中溶液(酸性)由红棕色变浅绿色的原因Fe3+消耗SO32-,c(SO32-)减小,平衡Fe2+(aq)+SO32-(aq)?FeSO3(s)(墨绿色)逆向移动,溶液颜色由红棕色变为浅绿色.
14.下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:(除特别注明外,其它一律用化学式表示)
(1)化学性质最不活泼的单质是Ne,最高价氧化物水化物中碱性最强的是KOH.
(2)属于过渡元素的是G(填字母),H在周期表中的位置第三周期第ⅥA族.
(3)某元素二价阳离子的核外有10个电子,该元素是镁(填元素名称)
(4)L、M、T形成的气态氢化物化合物稳定性由强到弱的顺序H2O>NH3>PH3,J、L、H的最高价氧化物对应水化物的酸性由强到弱的顺序H2SO4>H3PO4>H2SiO3.
(5)D、M、W、E原子半径由大到小的顺序Ca>Mg>C>O.
(6)写出Z单质与B最高价氧化物对应水化物相互反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
| A | |||||||||||||||||
| W | T | M | F | ||||||||||||||
| B | D | Z | J | L | H | V | |||||||||||
| C | E | G | Q | ||||||||||||||
(2)属于过渡元素的是G(填字母),H在周期表中的位置第三周期第ⅥA族.
(3)某元素二价阳离子的核外有10个电子,该元素是镁(填元素名称)
(4)L、M、T形成的气态氢化物化合物稳定性由强到弱的顺序H2O>NH3>PH3,J、L、H的最高价氧化物对应水化物的酸性由强到弱的顺序H2SO4>H3PO4>H2SiO3.
(5)D、M、W、E原子半径由大到小的顺序Ca>Mg>C>O.
(6)写出Z单质与B最高价氧化物对应水化物相互反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
11.如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )
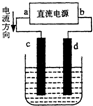

| A. | a为负极、b为正极 | B. | c电极上发生还原反应 | ||
| C. | 电解过程中,d电极质量增加 | D. | 电解过程中,氯离子浓度不变 |
18.元素周期律和元素周期表是学习化学的重要工具,下列叙述不正确的是( )
| A. | 元素周期表共18列,从左到右的第十七列为卤族元素 | |
| B. | 同一周期元素的原子,半径越小越容易失去电子 | |
| C. | 副族元素全部是金属元素 | |
| D. | 在过渡元素中,人们可以寻找到各种优良的催化剂和高温、耐腐蚀的合金材料 |
8.如图各装置能构成原电池的是( )
| A. |  | B. |  | C. |  | D. |  |
15.下列化合物中含有离子键的是( )
| A. | CO2 | B. | NaCl | C. | CH4 | D. | H3PO4 |
12.氮气化学性质稳定的原因是 ( )
| A. | 氮的非金属性弱 | B. | 氮气的熔沸点低 | ||
| C. | 氮原子半径较小 | D. | 氮分子中原子间共价键不易断裂 |
13.某固体KOH样品含H2O 7.55%、含K2CO3 4.32%,将a g此样品与bmL 1mol/L盐酸反应完全,再用c mol/L KOH溶液25.12mL恰好使剩余盐酸中和.所得的溶液蒸干后,固体的质量为( )
| A. | 0.8a g | B. | 0.0745b g | C. | 0.0376c g | D. | 无法计算 |