题目内容
【题目】下列离子方程式书写正确旳是 ( )
A.碳酸氢铵和足量旳氢氧化钠溶液反应:NH4++OH-=NH3↑+H2O
B.三氯化铁溶液中通入硫化氢气体:2Fe3++H2S=2Fe2++S↓+2H+
C.用稀硝酸浸泡做过银镜反应旳试管:Ag+2H++NO3-=Ag++NO2↑+H2O
D.偏铝酸钠溶液中通入过量旳二氧化碳气体:2AlO2-+CO2+2H2O=2Al(OH)3↓+CO32-
【答案】B
【解析】
A.碳酸氢铵和足量的氢氧化钠溶液反应,离子方程式:HCO3+NH4++2OH![]() NH3↑+2H2O+CO32,故A错误;
NH3↑+2H2O+CO32,故A错误;
B.三氯化铁溶液中通入硫化氢气体,离子方程式:2Fe3++H2S=2Fe2++S↓+2H+,故B正确;
C.用稀硝酸浸泡做过银镜反应的试管,离子方程式:3Ag+4H++NO3=3Ag++NO↑+2H2O,故C错误;
D.偏铝酸钠溶液中通入过量的二氧化碳气体,离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故D错误;
故答案选B。

【题目】X、Y、Z、W是短周期中的四种常见元素,其相关信息如表:
元素 | 相关信息 |
X | X最外层电子数是次外层电子数的3倍 |
Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
Z | Z和Y同周期,Z的非金属性大于Y |
W | W的一种核素的质量数为23,中子数为12 |
(1)Y位于元素周期表第________周期________族,Y和Z的最高价氧化物对应的水化物的酸性较强的是________(填化学式)。
(2)Z的简单离子的电子式为________。
(3)W可以与X形成两种化合物,写出这两种化合物的电子式:__________________、____________________。
【题目】汽车发动机工作时会产生包括CO、NOx等多种污染气体,如何处理这些气体,对保护大气环境意义重大,回答下列问题:
(1)已知:2NO2(g) ![]() 2NO(g)+O2(g) ΔH1=+115.2 kJ·mol-1;
2NO(g)+O2(g) ΔH1=+115.2 kJ·mol-1;
2O3(g) ![]() 3O2(g) ΔH2=-286.6 kJ·mol-1。
3O2(g) ΔH2=-286.6 kJ·mol-1。
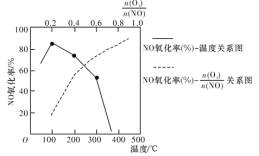
写出臭氧与NO作用产生NO2和O2的热化学方程式:___________。恒容密闭体系中NO氧化率随![]() 值的变化以及随温度的变化曲线如图所示。NO氧化率随
值的变化以及随温度的变化曲线如图所示。NO氧化率随![]() 值增大而增大的主要原因是________________________。
值增大而增大的主要原因是________________________。
(2)实验测得反应2NO(g)+O2(g) ![]() 2NO2(g) △H<0的即时反应速率满足以下关系式:v正=k正·c2(NO)·c(O2);v逆=k逆·c2(NO2),k正、k逆为速率常数,受温度影响
2NO2(g) △H<0的即时反应速率满足以下关系式:v正=k正·c2(NO)·c(O2);v逆=k逆·c2(NO2),k正、k逆为速率常数,受温度影响
①温度为T1时,在1L的恒容密闭容器中,投入0.6 molNO和0.3 molO2达到平衡时O2为0.2 mol;温度为T2时,该反应存在k正=k逆,则T1_______ T2 (填“大于”、“小于”或“等于”)。
②研究发现该反应按如下步骤进行:
第一步:NO+NO![]() N2O2 快速平衡 第二步:N2O2 +O2
N2O2 快速平衡 第二步:N2O2 +O2![]() 2NO2 慢反应
2NO2 慢反应
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v1正=k1正×c2(NO);v1逆=k1逆×c(N2O2)
下列叙述正确的是______
A.同一温度下,平衡时第一步反应的![]() 越大反应正向程度越大
越大反应正向程度越大
B.第二步反应速率低,因而转化率也低
C.第二步的活化能比第一步的活化能低
D.整个反应的速率由第二步反应速率决定
(3)科学家研究出了一种高效催化剂,可以将CO和NO2两者转化为无污染气体,反应方程式为:2NO2(g)+4CO(g) ![]() 4CO2(g)+N2(g) △H<0
4CO2(g)+N2(g) △H<0
某温度下,向10L密闭容器中分别充入0.1molNO2和0.2 molCO,发生上述反应,随着反应的进行,容器内的压强变化如下表所示:
时间/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
压强/kPa | 75 | 73.4 | 71.95 | 70.7 | 69.7 | 68.75 | 68.75 |
回答下列问题:
①在此温度下,反应的平衡常数Kp=_________kPa-1(Kp为以分压表示的平衡常数,计算结果精确到小数点后2位);若保持温度不变,再将CO、CO2气体浓度分别增加一倍,则平衡_____(填“右移”或“左移”或“不移动”);
②若将温度降低,再次平衡后,与原平衡相比体系压强(p总)如何变化?_______(填“增大”、“减小”或“不变”),原因是_____________________。
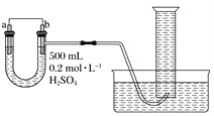
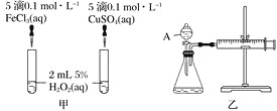
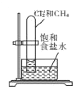
【题目】下述实验方案能达到实验结果的是( )
编号 | A | B | C | D |
实验方案 |
|
片刻后在 |
|
置于光亮处 |
实验结果 | 铁钉发生析氢反应 |
| 左球气体颜色加深; 右球气体颜色变浅 | 甲烷与氯气发生加成反应 |
A.AB.BC.CD.D
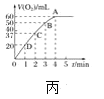
【题目】在一定温度下,10mL 0.40mol/L H2O2 溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:υ(H2O2)=3.3×10-2mol/(L·min)
B.6~10min的平均反应速率:υ(H2O2)<3.3×10-2mol/(L·min)
C.反应到6min时,c(H2O2)=0.30mol/L
D.反应到6min时,H2O2 分解了50%