题目内容
【题目】下述实验方案能达到实验结果的是( )
编号 | A | B | C | D |
实验方案 |
|
片刻后在 |
|
置于光亮处 |
实验结果 | 铁钉发生析氢反应 |
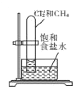
| 左球气体颜色加深; 右球气体颜色变浅 | 甲烷与氯气发生加成反应 |
A.AB.BC.CD.D
【答案】C
【解析】
A.铁钉在中性或碱性条件发生吸氧腐蚀,在酸性条件下发生析氢反应,故A不符;
B.![]() 电极是阳极,更易腐蚀,得不到保护,故B不符;
电极是阳极,更易腐蚀,得不到保护,故B不符;
C.2NO2(g)![]() N2O4(g)为放热反应,热水中平衡向着逆向移动,二氧化氮浓度增大,左球气体颜色加深;冷水中平衡向着正向移动,二氧化氮浓度减小,右球气体颜色变浅,故C符合;
N2O4(g)为放热反应,热水中平衡向着逆向移动,二氧化氮浓度增大,左球气体颜色加深;冷水中平衡向着正向移动,二氧化氮浓度减小,右球气体颜色变浅,故C符合;
D.甲烷中没有不饱和键,不能与氯气发生加成反应,在光照条件下,甲烷与氯气发生取代反应,故D不符;
故选C。

练习册系列答案
相关题目