题目内容
【题目】Ⅰ、物质变化观念是化学学科核心素养之一。已知a、b、c、d、e五种物质的相互转化关系如图所示,其中a、d、e为常见的单质,b、c为化合物。
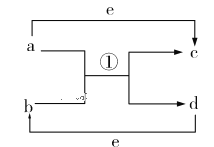
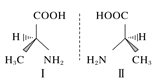
(1)若a、d为短周期非金属单质,且a、d所含元素同主族,a、e所含元素在不同周期。则b、c的沸点:b_________c(填“<”“>”或“=”);a和b反应生成两种氧化物的化学方程式为_________________。
(2)若a是常见的金属单质,点燃发出耀眼白光。d为固态非金属单质,熔点很高,其某种形态单质硬度极大,e为常见的气体单质,则a和b反应的化学方程式为________________________________。
(3)若a、d为常见的金属单质,它们与浓硝酸在加热条件下才能顺利反应。a既可以与强酸反应也可以与强碱反应,d在e中燃烧可以生成b。则足量的d与稀硝酸反应的离子方程式为__________________________________________。
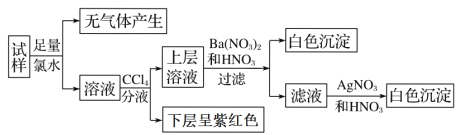
Ⅱ、HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(4)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2)则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填字母)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(5)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:________________________________________________。
【答案】< 2H2S +3O2![]() 2SO2 +2H2O 2Mg+CO2
2SO2 +2H2O 2Mg+CO2![]() 2MgO+C 3Fe+8H++2
2MgO+C 3Fe+8H++2![]()
![]() 3Fe2++2NO↑ +4H2O D NO
3Fe2++2NO↑ +4H2O D NO![]() +Cl2+H2O===NO3-+2H++2Cl-
+Cl2+H2O===NO3-+2H++2Cl-
【解析】
Ⅰ、(1)若a、d为短周期非金属单质,且a、d所含元素同主族,则a为O2、d为S;a、e所含元素在不同周期,则e为H2。H2S分子间不能形成氢键,而H2O分子间可形成氢键,从而得沸点关系出b<c;O2和H2S反应生成H2O和SO2。
(2)若a是常见的金属单质,点燃发出耀眼白光,则其为镁。d为固态非金属单质,熔点很高,其某种形态单质硬度极大,则其为碳,则b为CO2,c为MgO,从而得出e为O2,由此可得出a和b反应的化学方程式。
(3)若a、d为常见的金属单质,它们与浓硝酸在加热条件下才能顺利反应,言外之意是在常温下反应不能顺利进行,则a为Al,d为Fe。Fe在O2中燃烧可以生成Fe3O4。足量的Fe与稀硝酸反应,生成Fe(NO3)2、NO和H2O。
Ⅱ、(4)A.亚硝酸盐能将Fe2+转化为Fe3+,则其作氧化剂,被还原,A正确;
B.维生素C能将Fe3+转化为Fe2+,则其为还原剂,B正确;
C.维生素C作为还原剂,能将Fe3+还原为Fe2+,C正确;
D.亚硝酸盐将Fe2+转化为Fe3+,则其是氧化剂,D错误。
(5)新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,依题意可写出反应的离子方程式。
Ⅰ、(1)若a、d为短周期非金属单质,且a、d所含元素同主族,则a为O2、d为S;a、e所含元素在不同周期,则e为H2。H2S分子间不能形成氢键,而H2O分子间可形成氢键,从而得出b、c的沸点关系为b<c;O2和H2S反应化学方程式为2H2S +3O2![]() 2SO2 +2H2O。答案为:<;2H2S +3O2
2SO2 +2H2O。答案为:<;2H2S +3O2![]() 2SO2 +2H2O;
2SO2 +2H2O;
(2)若a是常见的金属单质,点燃发出耀眼白光,则其为镁。d为固态非金属单质,熔点很高,其某种形态单质硬度极大,其为碳,则b为CO2,c为MgO,从而得出e为O2,由此可得出a和b反应的化学方程式为2Mg+CO2![]() 2MgO+C。答案为:2Mg+CO2
2MgO+C。答案为:2Mg+CO2![]() 2MgO+C;
2MgO+C;
(3)若a、d为常见的金属单质,它们与浓硝酸在加热条件下才能顺利反应,言外之意是在常温下反应不能顺利进行,则a为Al,d为Fe。Fe在O2中燃烧可以生成Fe3O4。足量的Fe与稀硝酸反应的离子方程式为3Fe+8H++2![]() =3Fe2++2NO↑ +4H2O。答案为:3Fe+8H++2
=3Fe2++2NO↑ +4H2O。答案为:3Fe+8H++2![]() =3Fe2++2NO↑ +4H2O;
=3Fe2++2NO↑ +4H2O;
Ⅱ、(4)A.亚硝酸盐能将Fe2+转化为Fe3+,则其作氧化剂,被还原,A正确;
B.维生素C能将Fe3+转化为Fe2+,则其为还原剂,B正确;
C.维生素C作为还原剂,能将Fe3+还原为Fe2+,C正确;
D.亚硝酸盐将Fe2+转化为Fe3+,则其是氧化剂,D错误。答案为:D;
(5)新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,依题意可得反应的离子方程式为NO![]() +Cl2+H2O==NO3-+2H++2Cl-。答案为:NO
+Cl2+H2O==NO3-+2H++2Cl-。答案为:NO![]() +Cl2+H2O==NO3-+2H++2Cl-。
+Cl2+H2O==NO3-+2H++2Cl-。

【题目】锌灰是炼锌厂的烟道灰,含ZnO 35%以上,还含有少量的氧化锰(MnO)、氧化铜、 铁的氧化物和不溶于酸的杂质,工业上常用酸浸法回收 ZnSO4·7H2O。已知 ZnSO4·7H2O 晶体易溶于水,难溶于酒精,某兴趣小组实验室模拟回收 ZnSO4·7H2O 晶体,流程如下:

请回答:
(1)分析步骤 II 中的操作和原理, 回答下列问题:
①结合表 1、 2,分析选择的 pH 及温度分别是______________________, 其中, 可以采用加入_________________________来调节 pH ;
表1 pH对ZnSO4.7H2O 回收量及纯度的影响
pH | ZnSO4.7H2O 回收量(g) | 产品中Fe的含量% | 产品中其他重金属含量% |
1 | 114.32 | 0.750 | 0.059 |
2 | 114.4 | 0.086 | 0.056 |
3 | 113.68 | 0.034 | 0.054 |
4 | 113.60 | 0.010 | 0.050 |
5 | 112.43 | 0.010 | 0.050 |
表2 温度对ZnSO4.7H2O 回收量及纯度的影响
温度 (℃) | ZnSO4.7H2O 回收量(g) | 产品中F的含量% | 产品中其他重金属含量% |
20 | 111.45 | 0.011 | 0.052 |
40 | 112.89 | 0.010 | 0.051 |
60 | 113.30 | 0.010 | 0.050 |
80 | 113.80 | 0.010 | 0.050 |
90 | 114.40 | 0.091 | 0.048 |
②酸性 KMnO4 溶液将溶液中的 Fe2+氧化,生成两种沉淀;同时,过量的高锰酸钾在微酸性的条件能自动分解生成MnO2 沉淀。试写出在该环境下,KMnO4 溶液氧化 Fe2+的离子反应方程式_________________________________________。 若用稀硝酸做氧化剂,除了产物中可能含有 Zn(NO3)2 外,还可能的缺点是:_________________________;
(2)分析整个实验过程中,回答下列问题:
①滤渣 B 的主要成分为___________________________;
②如何检验滤液B中是否含有铁元素_____________________________________;
③写出生成滤渣C的离子方程式__________________________________________;
(3)为测定 ZnSO4·7H2O 晶体的纯度,可用 K4Fe(CN)6 标准液进行滴定。主要原理如下:2K4Fe(CN)6+ 3ZnSO4= K2Zn3[Fe(CN)6]2↓+ 3K2SO4
准确称取 5.000g ZnSO4·7H2O 晶体,用蒸馏水溶解并定容至 250mL,准确移取该溶液 25.00mL至锥形瓶中,用 0.0500mol/L K4Fe(CN)6 溶液进行滴定,所得数据如下表:
实验次数 | 滴定前读数/mL | 滴定后读数/mL |
1 | 0.10 | 19.92 |
2 | 1.34 | 21.12 |
3 | 0.00 | 20.10 |
则 ZnSO4·7H2O 晶体的纯度是_______________(以质量分数表示,保留到小数点后两位)。