题目内容
【题目】氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成都需要用它。
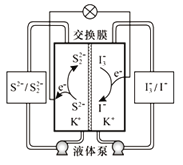
(1)工业上通常采用电解法制氯气,请观察图后回答下列问题:

①请写出该反应的化学方程式____。
②通电后,b侧产生的气体是____![]() 填化学式
填化学式![]() 。
。
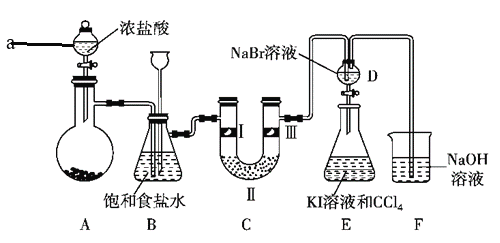
(2)某学生设计如图所示的实验装置,利用浓盐酸和二氧化锰固体制取氯气,并与潮湿的消石灰反应制取少量漂白粉![]() 这是一个放热反应
这是一个放热反应![]() ,回答下列问题:
,回答下列问题:

①漂白粉将在B装置的U形管中产生,其化学方程式是_____。
②装置C的作用是___。
(3)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3) 2,为避免此副反应的发生,可采取的措施是___。
②为避免另一个副反应的发生,可将装置作何改进___ 。
③家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是____。
A.食盐 B.食醋 C.烧碱 D.纯碱
【答案】2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ Cl2 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 吸收未反应完的氯气,防止污染空气 冷却B装置 A和B之间连接一个装有饱和氯化钠溶液的洗气瓶 B
2NaOH+H2↑+Cl2↑ Cl2 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 吸收未反应完的氯气,防止污染空气 冷却B装置 A和B之间连接一个装有饱和氯化钠溶液的洗气瓶 B
【解析】
(1)电解饱和食盐水可以得到氢氧化钠、氯气和氢气;b是阳极,b侧产生的气体是氯气;
(2)A中:发生反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,B中:氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水;C中:氯气有毒,不能直接排放到空气中,需要进行尾气吸收;
MnCl2+Cl2↑+2H2O,B中:氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水;C中:氯气有毒,不能直接排放到空气中,需要进行尾气吸收;
(3)依据信息可知温度较高时氯气与消石灰反应生成Ca(ClO3)2,为为避免此副反应的发生应降低温度;
挥发出的氯化氢能够与氢氧化钙发生酸碱中和反应;要避免此反应的发生应该除去氯气中的氯化氢;酸性条件下,漂白粉的氧化性更强。
(1)①电解饱和食盐水可以得到氢氧化钠、氯气和氢气,反应的化学方程式2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
②通电后,b是阳极,b侧产生的气体是Cl2;
(2)A中:发生反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,B中:氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水;
MnCl2+Cl2↑+2H2O,B中:氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水;
①漂白粉将在B装置的U形管中产生,其化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
②氯气有毒,不能直接排放到空气中,装置C的作用是吸收未反应完的氯气,防止污染空气;
(3)①依据信息可知温度较高时氯气与消石灰反应生成Ca(ClO3)2,为为避免此副反应的发生应该冷却B装置;
②挥发出的氯化氢能够与氢氧化钙发生酸碱中和反应,要避免此反应的发生应该除去氯气中的氯化氢,可以在A与B之间连接一个装有饱和氯化钠溶液的洗气瓶;
③酸性条件下,漂白粉的氧化性更强,家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是食醋,故选B。

【题目】氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。某实验小组以H2O2分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下按照下表所示的方案完成实验。
实验编号 | 温度(℃) | 反应物 | 催化剂 |
① | 20 | 25 mL 3% H2O2溶液 | 无 |
② | 20 | 25 mL 5% H2O2溶液 | 无 |
③ | 20 | 25 mL 5% H2O2溶液 | 0.1g MnO2 |
④ | 20 | 25 mL 5% H2O2溶液 | 1~2滴1mol/L FeCl3溶液 |
⑤ | 30 | 25 mL 5% H2O2溶液 | 0.1g MnO2 |
(1)实验①和②的目的是____________________________。同学甲在进行实验时并没有观察到明显现象。资料显示,通常条件下过氧化氢稳定,不易分解。为了达到实验目的,可采取的改进方法是__________(写出一种即可)。
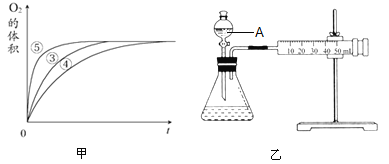
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如甲图所示。分析该图能得出的结论是__________________________,__________________________;
(3)写出实验③中H2O2分解的化学方程式:______________________________;
(4)同学乙设计了乙图所示的实验装置对过氧化氢的分解速率进行定量分析。以生成10mL气体为准,其他影响实验的因素均已忽略。图中仪器A的名称为__________,实验中需要测量的数据是______________。
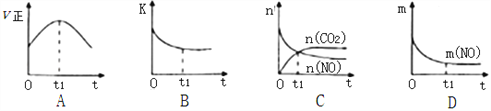
(5)某反应在体积为2L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知X、Y、Z均为气体).
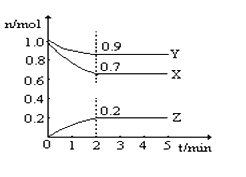
①该反应的化学方程式为______.
②反应开始至2分钟时,Y的平均反应速率为______.
③能说明该反应已达到平衡状态的是______
A.υ(X)=3υ(Y)B.容器内气体密度不变
C.υ逆(Z)=2υ正(Y)D.各组分的物质的量相等
E.混合气体的平均相对分子质量不再改变的状态
④由图求得平衡时X的转化率为______.
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2 mol的A和0.8 mol的B,反应初始4 s内A的平均反应速率υ(A)=0.005 mol/(L·s)。下列说法正确的是
A. 4 s时c(B)为0.38 mol/L
B. 830℃达平衡时,A的转化率为20%
C. 反应达平衡后,升高温度,平衡正向移动
D. 1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数为0.4
A(g)+B(g)的平衡常数为0.4