题目内容
12.下列说法正确的有( )| A. | 原电池是将电能转变为化学能的装置 | |
| B. | 原电池工作时,阳离子向负极方向移动 | |
| C. | 反应Cu+2H+=Cu2++H2↑可设计成原电池装置 | |
| D. | 锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率 |
分析 A、原电池是化学能转化为电能;
B、原电池工作时,阳离子向正极方向移动;
C、反应Cu+2H+=Cu2++H2↑不能自发发生;
D、形成原电池能加快反应速率.
解答 解:A、原电池是化学能转化为电能的装置,故A错误;
B、原电池工作时,阳离子向正极方向移动,故B错误;
C、反应Cu+2H+=Cu2++H2↑不能自发发生,所以不可设计成原电池装置,故C错误;
D、锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液,Zn置换出Cu,Zn与Cu、硫酸形成原电池,形成原电池能加快反应速率,故D正确;
故选D.
点评 本题考查了原电池原理,题目难度不大,注意把握原电池原理以及原电池的构成条件等.

练习册系列答案
相关题目
2.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 将足量CO2通入:NH4+、Na+、Al3+、NO${\;}_{3}^{-}$ | |
| B. | 在中性的水溶液中:Fe2+、K+、NO${\;}_{3}^{-}$、ClO- | |
| C. | 含有大量Al3+的溶液中:Na+、NO3-、Cl-、AlO2- | |
| D. | 水电离出的c(H+)=1×10-12mol•L-1的溶液中:Na+、Mg2+、HCO3-、SO${\;}_{4}^{2-}$ |
3.有机物分子式为C3H6,下列叙述正确的是( )
| A. | 一定是丙烯 | B. | 可能是丙烷 | C. | 可能是丙烯 | D. | 可能是丙炔 |
17.将4.05g Al投入到1mol/L NaOH溶液中,Al完全反应,至少需要NaOH溶液的体积和生成氢气的体积(标准状况)为( )
| A. | 225mL,5.04L | B. | 150mL,5.04L | C. | 225mL,3.36L | D. | 150mL,3.36L |
1.下列叙述正确的是( )
| A. | 一定温度和压强下,将 0.5mo1N2和 1.5mo1H2 置于密闭容器中充分反应生成 NH3(g),放 热 19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |||||||||
| B. | H2 标准燃烧热△H=-285.8 kJ•mol-1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ•mol-1 | |||||||||
| C. | C(石墨)═C(金刚石)△H=+1.9kJ•mol-1,说明石墨比金刚石稳定 | |||||||||
| D. | 通常人们把拆开 1 mol 某化学键所吸收的能量看成该化学键的键能:
|
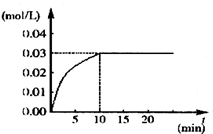 在某一容积为5L的密闭容器内,加入 0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:
在某一容积为5L的密闭容器内,加入 0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应: