题目内容
19.下列物质沸点最低的是( )| A. | 庚烷 | B. | 新戊烷 | C. | 正戊烷 | D. | 2-甲基丁烷 |
分析 烷烃中碳原子个数越多其熔沸点越高、密度越大,烷烃的同分异构体中支链越多其熔沸点越低,据此分析解答.
解答 解:烷烃中碳原子个数越多其熔沸点越高、密度越大,这几种烷烃中碳原子个数大小顺序是庚烷>新戊烷=正戊烷=2-甲基丁烷,所以庚烷熔沸点最高;
烷烃的同分异构体中支链越多其熔沸点越低,新戊烷、正戊烷和2-甲基丁烷属于同分异构体,新戊烷有两个支链、2-甲基戊烷有一个支链、正戊烷没有支链,所以这几种物质的熔沸点正戊烷>2-甲基丁烷>正戊烷,
所以熔沸点最低的是新戊烷,故选B.
点评 本题考查烷烃熔沸点高低判断,明确烷烃熔沸点高低与碳原子个数、支链的关系即可解答,题目难度不大.

练习册系列答案
相关题目
9.下列各组中两种微粒所含电子数不相等的是( )
| A. | H3O+ 和OH- | B. | CO和N2 | C. | HNO2和NO2- | D. | CH3+ 和NH4+ |
10.某学习小组进行了如图所示的实验,实验后组员之间的交流不合理的是( )
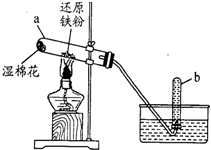

| A. | 甲同学认为试管b中收集到的气体可点燃,且产生淡蓝色火焰 | |
| B. | 乙同学认为试管a中生成的黑色固体可能为四氧化三铁 | |
| C. | 丙同学认为将少量还原性铁粉放入试管中,加适量的水,加热也可实现该反应 | |
| D. | 丁同学认为可用盐酸和KSCN溶液来验证产物中的三价铁 |
7.下列物质中,既含离子键、又含极性共价键的是( )
| A. | NaOH | B. | Na2O | C. | HCl | D. | CaCl2 |
14.下列实验操作中正确的是( )
| A. | 将溴水、铁粉和苯混合加热即可制得溴苯 | |
| B. | 除去溴苯中红棕色的溴,可用稀NaOH溶液反复洗涤,再用分液漏斗分液 | |
| C. | 用苯和浓HNO3、浓H2SO4反应制取硝基苯时需水浴加热,温度计应放在反应混合液中 | |
| D. | 制取硝基苯时,应先向试管中加入浓H2SO4 2 mL,再加入1.5 mL浓HNO3,再滴入苯约1 mL,然后放在水浴中加热 |
4.设NA为阿伏加德罗常数,则下列说法正确的是( )
| A. | 一定条件下,2.3g Na完全与O2反应生成3.6g产物时得到的电子数为0.1NA | |
| B. | 1L 0.1mol醋酸溶液中所含分子数少于0.1NA | |
| C. | 水分子中1mol羟基含有的电子总数为9NA | |
| D. | 1 mol H2O2含有极性共价键键数为NA,含有非极性共价键为键数2NA |
11.下列说法正确的是( )
| A. | 2149421494Pu位于周期表中第六周期 | |
| B. | 1315313153 I与1255312553I性质完全相同 | |
| C. | 1315313153I与1255312553I 互为同位素 | |
| D. | 1315313153I的质子数为78 |
7.标准状况下,将VLH2S气体通入a Lb mo l/L的 NaOH 溶液中,下列对所得溶液的描述不正确的是( )
| A. | 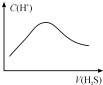 随着 H2S气体的通入,溶液中由水电离出的c(H+)有如图变化关系 | |
| B. | 当V22.4=a b时,所得溶液中存在:c(OH-)+c(S2-)=c(H+)+c(H2S) | |
| C. | 当V11.2=a b时,所得溶液中存在:c(Na+)>c(S2-)>c(OH-)>c(HS-)>c( H+) | |
| D. | 当V22.4<a b<V11.2时,所得溶液中一定存在:c(Na+)=c(S2-)+c(HS-)+c(H2S) |

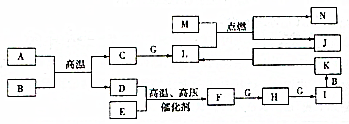 已知A、B、C、F、H、I、K、L、N是化合物,且A、B、F分子中电子数相等,D、E、G、J、M为单质,M为金属,J为黑色粉末,各物质转化关系如图所示,请回答:
已知A、B、C、F、H、I、K、L、N是化合物,且A、B、F分子中电子数相等,D、E、G、J、M为单质,M为金属,J为黑色粉末,各物质转化关系如图所示,请回答: