题目内容
8.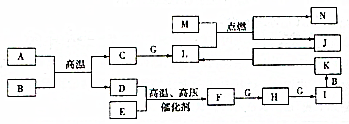 已知A、B、C、F、H、I、K、L、N是化合物,且A、B、F分子中电子数相等,D、E、G、J、M为单质,M为金属,J为黑色粉末,各物质转化关系如图所示,请回答:
已知A、B、C、F、H、I、K、L、N是化合物,且A、B、F分子中电子数相等,D、E、G、J、M为单质,M为金属,J为黑色粉末,各物质转化关系如图所示,请回答:(1)写出下列反应的化学方程式:M+L→N+J2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO;F+G→H4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)已知16g气体A与足量的气体G完全反应,生成气体C和液体B,同时放出Q kJ的热量,写出该反应的热化学方程式:2CH4(g)+3O2(g)=2CO(g)+4H2O(g)△H=-2QJK/mol;
(3)等物质的量的K与F反应,所得溶液中离子浓度大小顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-).
分析 M为金属,J为黑色粉末,L是化合物,M能在L中点燃生成J,则可推断L为CO2,M为Mg,N为MgO,J为C,C和G能生成L,且G是单质,C是化合物,可推断G为O2,C为CO,A、B分子中电子数相等,且都是化合物,D为单质,A、B高温生成C和D,则A为CH4,B为H2O,D为H2,D和E高温高压催化剂条件下生成F,F与A、B的电子数相同,则E为N2,F为NH3,F与G反应生成H为NO,I为NO2,所以K为HNO3,浓硝酸与碳反应生成二氧化碳,物质之间均符合图中转化,据此答题.
解答 解:M为金属,J为黑色粉末,L是化合物,M能在L中点燃生成J,则可推断L为CO2,M为Mg,N为MgO,J为C,C和G能生成L,且G是单质,C是化合物,可推断G为O2,C为CO,A、B分子中电子数相等,且都是化合物,D为单质,A、B高温生成C和D,则A为CH4,B为H2O,D为H2,D和E高温高压催化剂条件下生成F,F与A、B的电子数相同,则E为N2,F为NH3,F与G反应生成H为NO,I为NO2,所以K为HNO3,浓硝酸与碳反应生成二氧化碳,物质之间均符合图中转化,
(1)M+L→N+J的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,F+G→H的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO;4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)已知16g(即1mol)CH4与足量的氧气完全反应,生成气体一氧化碳和液体水,同时放出Q kJ的热量,该反应的热化学方程式为2CH4(g)+3O2(g)=2CO(g)+4H2O(g)△H=-2QJK/mol,
故答案为:2CH4(g)+3O2(g)=2CO(g)+4H2O(g)△H=-2QJK/mol;
(3)F为NH3,K为HNO3,等物质的量的K与F反应,所得溶液硝酸铵溶液,铵根离子水解显酸性,溶液中离子浓度大小顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-),故答案为:c(NO3-)>c(NH4+)>c(H+)>c(OH-).
点评 本题考查无机物的推断,把握甲烷与水高温下反应生成CO和氢气为解答的难点,熟悉合成氨反应、Mg与二氧化碳反应、C与浓硝酸的反应为解答的关键,侧重物质的性质及相互转化的考查,题目难度较大.

| A. | 庚烷 | B. | 新戊烷 | C. | 正戊烷 | D. | 2-甲基丁烷 |
| A. | 16O2与18O2互为同分异构体 | |
| B. | 16O与18O核外电子排布方式相同 | |
| C. | 通过化学变化可以实现16O与18O间的相互转化 | |
| D. | 1.12 L 16O2和1.12 L 18O2均含0.1NA个氧原子 |
| A. | 酸性高锰酸钾 | B. | 溴水 | C. | 液溴 | D. | NaOH溶液 |
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强 d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为氩,氧化性最弱的简单阳离子是Na+.
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
制铝时,电解Al2O3而不电解AlCl3的原因是氯化铝是共价化合物,熔融态氯化铝难导电.
(4)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
写出SiCl4的结构式:
 ;
;(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是b.
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1.写出该反应的化学方程式:4KClO3$\frac{\underline{\;400℃\;}}{\;}$KCl+3KClO4.
 硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害.
硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害.