题目内容
17.下列有关表示方法中,正确的是( )| A. | 次氯酸的电子式为: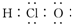 | |
| B. | 氮原子轨道表示式为: | |
| C. | 硫原子的最外层电子排布式为:3s23p4 | |
| D. | N2的结构式为::N≡N: |
分析 A.次氯酸是共价化合物,氧原子与氢原子、氯原子分别通过1对共用电子对结合;
B.2p轨道应优先占据空轨道;
C.硫原子的最外层为第3层并且有6个电子;
D.N2的结构式为:N≡N.
解答 解:A.次氯酸是共价化合物,氧原子与氢原子、氯原子分别通过1对共用电子对结合,结构式为H-O-Cl,故电子式为: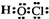 ,故A错误;
,故A错误;
B.2p轨道应优先占据空轨道,故B错误;
C.硫原子的最外层为第3层并且有6个电子,所以硫原子的最外层电子排布式为:3s23p4,故C正确;
D.N2的结构式为:N≡N,故D错误;
故选C.
点评 本题考查电子式的书写、轨道表示式、电子排布式以及结构式的判断,难度不大,注重基础知识的考查.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列关于镁的冶炼说法中,正确的是( )
| A. | 冶炼镁的最后一步反应为电解MgCl2溶液 | |
| B. | 由氯化镁的结晶水合物得到氯化镁属于物理变化 | |
| C. | 利用海水和石灰水作用可以得到氯化镁 | |
| D. | 利用氯化镁冶炼金属镁而不利用氧化镁的原因是氧化镁的熔点太高 |
8.下列说法错误的是( )
| A. | 石油和天然气的主要成分都是碳氢化合物 | |
| B. | 乙醇、乙酸和乙酸乙酯可以用饱和碳酸钠溶液鉴别 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 甘氨酸(NH2-CH2-COOH)既能与NaOH反应,又能与盐酸反应 |
5.常温下,下列溶液中微粒浓度关系一定正确的是( )
| A. | 氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) | |
| B. | pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) | |
| C. | 0.1 mol•L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) | |
| D. | 0.1 mol•L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
12.进行一氯取代反应后,只能生成三种沸点不同产物的烷烃是( )
| A. | (CH3)3CCH2CH3 | B. | (CH3CH2)2CHCH3 | C. | (CH3)2CHCH(CH3)2 | D. | (CH3)2CHCH2CH2CH3 |
2.下列各组中互为同位素的是( )
| A. | ${\;}_{19}^{40}$K与${\;}_{20}^{40}$Ca | B. | 正丁烷与异丁烷 | ||
| C. | ${\;}_{19}^{40}$K与${\;}_{19}^{39}$K | D. | 金刚石与石墨 |
9.下列纸层析实验示意图正确的是( )
| A. |  | B. |  | C. |  | D. |  |
7.下列说法正确的是( )
| A. | 分子晶体的熔点比金属晶体的低 | |
| B. | 在晶体中只要有阳离子,一定有阴离子 | |
| C. | 在SiO2晶体中,Si原子与Si-O键数目比为1:2 | |
| D. | 离子化合物中可能含有非极性共价键 |