题目内容
【题目】某学习小组为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。请补充完成该实验报告。
(1)(实验原理)
溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察_____,据此判断溶液中自由移动的离子浓度的变化,从而证明反应是离子反应。
(2)(实验装置)如图1所示。

(实验过程与记录)
实验步骤 | 实验现象 | 实验结论 |
连接好装置,向烧杯中加入25mL1molL﹣1的Ba(OH)2溶液和2滴酚酞溶液,逐滴滴加1molL﹣1的H2SO4溶液直至过量,边滴边振荡。 | (2)_____(填写支持实验结论的证据) | Ba(OH)2溶液和H2SO4溶液的反应是离子反应 |
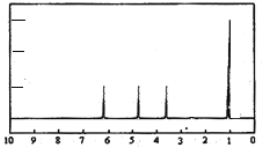
(3)整个过程中混合溶液的导电能力(用电流强度Ⅰ表示)可近似地用图2中的_____(填序号)曲线表示。
(4)下列三种情况下,与上述实验中离子方程式相同的是_____。
A 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42﹣恰好完全沉淀
B 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至至溶液显中性
C 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(5)已知:PbSO4难溶于水,但可溶于醋酸氨溶液中形成无色溶液,其化学方程式为:PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4.写出该反应的离子方程式为_____。
【答案】灯泡的明暗程度 灯泡由明变暗,直至熄灭,然后又逐渐变亮 c B PbSO4+2CH3COO-=(CH3COO)2Pb+SO42-
【解析】
(1)溶液的导电性由溶液中离子的浓度及离子电荷数决定,灯泡的明暗程度反映了离子浓度的变化;
(2)向Ba(OH)2溶液中逐滴滴加H2SO4溶液直至过量,根据溶液中离子浓度的变化可知灯泡的明暗的变化,从而证明发生了离子反应;
(3)同(2);
(4)A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42﹣恰好完全沉淀,两者物质的量相等;
B 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至至溶液显中性,n(H+)=n(OH-);
C 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量,NaHSO4少量;
(5)PbSO4难溶于水,但可溶于醋酸氨溶液中形成无色溶液,说明(CH3COO)2Pb是弱电解质。
(1)离子浓度越大,电荷越多,会使灯泡越亮,所以灯泡的明暗程度可以判断离子浓度变化。故答案为:灯泡的明暗程度;
(2)烧杯中开始只有强电解质Ba(OH)2,灯泡亮,然后随着加入H2SO4溶液,析出沉淀,离子浓度下降,所以会逐渐变暗,当完全中和时,会熄灭,再加入硫酸,由于H2SO4强电解质灯泡会逐渐变亮。故答案为:灯泡由明变暗,直至熄灭,然后又逐渐变亮;
(3)烧杯中开始只有强电解质Ba(OH)2,导电能力强,随着加入H2SO4溶液,析出沉淀同时生成水,离子浓度下降,导电能力减弱,当完全中和时,导电能力最弱。再加入时由于H2SO4强电解,导电能力又增强,所以用曲线c表示,故答案为:c;
(4) 实验中的离子方程式为: 2OH-+2H++Ba2++SO42-=2H2O+BaSO4↓;
A. 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42﹣恰好完全沉淀淀,二者物质的量相等,发生反应的离子方程式为:OH-+H++Ba2++SO42-=H2O+BaSO4↓,不满足,故A错误;
B. 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性,氢离子与氢氧根离子的物质的量相等,发生反应的离子方程式为:2OH-+2H++Ba2++SO42-=2H2O+BaSO4↓,满足条件,故B正确;
C. 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量,离子方程式按照硫酸氢钠的化学式组成书写,该反应的离子方程式为:OH-+H++Ba2++SO42-=H2O+BaSO4↓,不满足条件,故C错误。
故选:B。
(5). PbSO4难溶于水,(CH3COO)2Pb为弱电解质,书写离子方程式时保留化学式,离子方程式为:PbSO4+2CH3COO-=(CH3COO)2Pb+SO42-,故答案为:PbSO4+2CH3COO-=(CH3COO2)Pb+SO42-

【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中Fe+Cu2+===Cu+Fe2+ | 将Na加入到CuSO4溶液中2Na+Cu2+===Cu+2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应至中性2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和碘单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O===CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO |
A. A B. B C. C D. D