题目内容
【题目】下列说法中正确的是( )
A.1 mol S和O2的摩尔质量都是32 g
B.23g NO2和N2O4的混合气体中所含的O原子数为NA
C.1 mol任何气体中都含有相同的原子数
D.22.4 L CO2气体中含有3NA个原子
【答案】B
【解析】
A.S和O2的摩尔质量与物质的量大小无关,二者的摩尔质量都是32g/mol,故A错误;
B.23g NO2和N2O4的混合气体中含有NO2原子团的物质的量=![]() =0.5mol,所含的O原子数为0.5mol ×2×NA /mol=NA,故B正确;
=0.5mol,所含的O原子数为0.5mol ×2×NA /mol=NA,故B正确;
C.气体分子有单原子、双原子和多原子分子,则1mol气体中含有原子数不一定相等,故C错误;
D.未注明是否为标准状况,不能使用标况下的气体摩尔体积计算,故D错误;
故选B。

 阅读快车系列答案
阅读快车系列答案【题目】某学习小组为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。请补充完成该实验报告。
(1)(实验原理)
溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察_____,据此判断溶液中自由移动的离子浓度的变化,从而证明反应是离子反应。
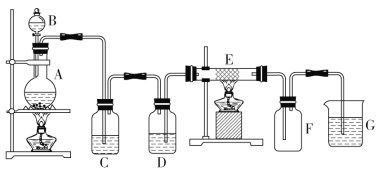
(2)(实验装置)如图1所示。

(实验过程与记录)
实验步骤 | 实验现象 | 实验结论 |
连接好装置,向烧杯中加入25mL1molL﹣1的Ba(OH)2溶液和2滴酚酞溶液,逐滴滴加1molL﹣1的H2SO4溶液直至过量,边滴边振荡。 | (2)_____(填写支持实验结论的证据) | Ba(OH)2溶液和H2SO4溶液的反应是离子反应 |
(3)整个过程中混合溶液的导电能力(用电流强度Ⅰ表示)可近似地用图2中的_____(填序号)曲线表示。
(4)下列三种情况下,与上述实验中离子方程式相同的是_____。
A 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42﹣恰好完全沉淀
B 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至至溶液显中性
C 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(5)已知:PbSO4难溶于水,但可溶于醋酸氨溶液中形成无色溶液,其化学方程式为:PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4.写出该反应的离子方程式为_____。