题目内容
1.下列关于碳和硅的叙述中,不正确的是( )| A. | +4价氧化物都能与氢氧化钠溶液反应 | |
| B. | 单质在加热时都能与氧气反应 | |
| C. | 氧化物都能溶于水生成相应的酸 | |
| D. | 碳和硅两种元素都有能导电的单质 |
分析 A.二氧化硅、二氧化碳都是酸性氧化物;
B.硅与氧气反应生成二氧化硅,碳与足量氧气反应生成二氧化碳;
C.二氧化硅不溶于水;
D.石墨是导体,晶体硅是半导体.
解答 解:A.二氧化硅、二氧化碳都是酸性氧化物,与氢氧化钠反应分别生成硅酸钠和碳酸钠,故A正确;
B.单质在加热时都能与氧气反应,都能生成对应的氧化物,故B正确;
C.二氧化硅不溶于水,与水不反应,故C错误;
D.石墨是导体,晶体硅是半导体,故D正确;
故选C.
点评 本题考查了硅、碳及其化合物的性质,熟悉相关物质的性质即可解答,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
11.含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:
根据表中数据,下列判断错误的是( )
| 烷烃名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 沸点(℃) | -88.6 | -42.1 | 36.1 | |
| 燃烧热(kJ•mol-1) | 1560.7 | 2877.6 | 3535.6 |
| A. | 丁烷的沸点有可能在0℃以下 | |
| B. | 上述四种烷烃中戊烷最容易液化,打火机中所用的燃料就是戊烷 | |
| C. | 丙烷完全燃烧生成4mol气态水,所放出的热量小于2877.6kJ | |
| D. | 烷烃的含碳量越高,其燃烧热值也就越大 |
12.有镁、铝混合粉末25.5克,将它完全溶于600ml 5mol/L的盐酸溶液中,若要使沉淀质量达到最大值,则需加入2mol/L的氢氧化钠溶液的体积为( )
| A. | 1000 ml | B. | 500 ml | C. | 1500 ml | D. | 100 ml |
9.定条件下发生如下反应并达到平衡:X(g)+Y(g)?2Z(g) 该反应是放热反应.当达到新平衡后,降低温度,下列叙述正确的是( )
| A. | 正反应速率加快 | B. | 正反应速率减慢 | C. | 逆反应速率加快 | D. | 无法判断 |
16.下列说法正确的是( )
| A. | 原硅酸是白色胶状物,失去部分水后变成白色粉末状硅酸 | |
| B. | SiO2分子由一个硅原子和两个氧原子构成 | |
| C. | SiO2溶于水后则慢慢生成硅酸 | |
| D. | SiO2既能与酸反应,又能与强碱反应,故它是两性氧化物 |
6.足量的铝分别与等体积等物质的量浓度的盐酸和氢氧化钠溶液反应,产生气体的体积是(相同条件)( )
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 1:3 |
2.下列说法正确的是( )
| A. | 自然界中含有大量游离态的硅,纯净的硅晶体可用于制作计算机芯片 | |
| B. | Si、P、S、Cl相应的氧化物对应水化物的酸性依次增强 | |
| C. | 工业上通常用电解熔融氧化铝制得金属铝 | |
| D. | 金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表面形成氧化物薄膜,阻止反应的进一步发生 |
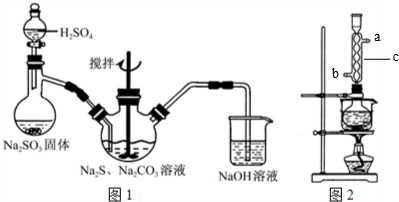
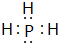 .
.