题目内容
欲除去下列物质中所含的杂质(括号内为杂质),请将选用的试剂或分离方法填在题后的横线上,并按要求写出有关反应的方程式.
(1)Na2CO3固体(NaHCO3);除杂试剂或方法 ,反应的化学方程式 .
(2)FeCl3溶液(FeCl2);除杂试剂 ,反应的离子方程式 .
(3)CO2(HCl);除杂试剂 ,反应的离子方程式 .
(1)Na2CO3固体(NaHCO3);除杂试剂或方法
(2)FeCl3溶液(FeCl2);除杂试剂
(3)CO2(HCl);除杂试剂
考点:物质的分离、提纯的基本方法选择与应用,离子方程式的书写,物质的分离、提纯和除杂
专题:离子反应专题
分析:(1)碳酸氢钠受热分解生成碳酸钠;
(2)氯化亚铁和氯气反应生成氯化铁;
(3)HCl与饱和碳酸氢钠反应生成二氧化碳.
(2)氯化亚铁和氯气反应生成氯化铁;
(3)HCl与饱和碳酸氢钠反应生成二氧化碳.
解答:
解:(1)碳酸氢钠受热分解生成碳酸钠,则利用加热法除杂,发生的反应为2NaHCO3
Na2CO3+CO2↑+H2O,故答案为:加热;2NaHCO3
Na2CO3+CO2↑+H2O;
(2)氯化亚铁和氯气反应生成氯化铁,则除杂试剂为氯气,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故答案为:氯气;2Fe2++Cl2═2Fe3++2Cl-;
(3)HCl与饱和碳酸氢钠反应生成二氧化碳,则除杂试剂为碳酸氢钠,发生的离子反应为HCO3-+H+═CO2↑+H2O,故答案为:碳酸氢钠;HCO3-+H+═CO2↑+H2O.
| ||
| ||
(2)氯化亚铁和氯气反应生成氯化铁,则除杂试剂为氯气,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故答案为:氯气;2Fe2++Cl2═2Fe3++2Cl-;
(3)HCl与饱和碳酸氢钠反应生成二氧化碳,则除杂试剂为碳酸氢钠,发生的离子反应为HCO3-+H+═CO2↑+H2O,故答案为:碳酸氢钠;HCO3-+H+═CO2↑+H2O.
点评:本题考查物质分离、提纯方法及选择,为高频考点,把握物质的性质及性质差异为解答的关键,注意混合物分离方法的选择和除杂的原则,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
工业上合成甲醇一般采用下列反应:CO(g)+2H(g)?CH30H(g)△H<0,下表是该反应在不同温度下的化学平衡常数(K):
则下列数据符合表中x的是( )
| 温度/℃ | 250 | 350 |
| K/(mol?L-2)-2 | 2.041 | x |
| A、0 | B、0.012 |
| C、32.081 | D、100 |
短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是( )
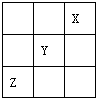

| A、X、Y、Z中X的单质最稳定 |
| B、Y的氢化物为HY |
| C、Z的最高价氧化物的化学式为ZO2 |
| D、能发生Cl2+H2Z═Z+2HCl的反应 |
下列各组微粒中,氧化性依次增强,且半径依次减小的是( )
| A、O、Cl、S、P |
| B、K+、Mg2+、Al3+、H+ |
| C、I-、Br-、Cl-、S2- |
| D、Al3+、Mg2+、Ca2+、Ba2+ |
在下列各溶液中,一定能大量共存的离子组是( )
| A、强酸性溶液中:K+、S2-、ClO-、SO42- |
| B、含有0.1mol?L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3- |
| C、室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
| D、加入Al能放出H2的溶液中::Na+、K+、CO32-、Cu2+ |
