题目内容
若除去氯气中少量的氯化氢气体,可选用的试剂是( )
| A、NaOH溶液 |
| B、AgNO3溶液 |
| C、饱和食盐水 |
| D、饱和Na2CO3溶液 |
考点:气体的净化和干燥,氯气的化学性质
专题:卤族元素
分析:除去氯气中少量的氯化氢气体,所选的试剂不能与氯气反应且能够除去氯化氢,如:氢氧化钠溶液、硝酸银溶液、饱和碳酸钠溶液;通常选用的试剂为饱和食盐水,因为氯气在饱和食盐水中溶解度较小,而氯化氢极易溶于饱和食盐水,据此可以除去装置氯化氢.
解答:
解:A.氢氧化钠溶液能够与氯气反应,不能用氢氧化钠溶液除去氯气中的氯化氢,故A错误;
B.氯气与水反应生成氯化氢和次氯酸,氯化氢能够与硝酸银溶液反应生成氯化银沉淀,即量取能够与硝酸银溶液反应,不能用硝酸银溶液除去氯化氢的氯化氢,故B错误;
C.氯气在饱和食盐水中溶解度较小,而氯化氢极易溶于饱和食盐水,可以用饱和食盐水除去氯气中的氯化氢气体,故C正确;
D.氯气能够与饱和碳酸钠溶液反应,不能用饱和碳酸钠溶液除去氯气中混有的装置氯化氢,故D错误;
故选C.
B.氯气与水反应生成氯化氢和次氯酸,氯化氢能够与硝酸银溶液反应生成氯化银沉淀,即量取能够与硝酸银溶液反应,不能用硝酸银溶液除去氯化氢的氯化氢,故B错误;
C.氯气在饱和食盐水中溶解度较小,而氯化氢极易溶于饱和食盐水,可以用饱和食盐水除去氯气中的氯化氢气体,故C正确;
D.氯气能够与饱和碳酸钠溶液反应,不能用饱和碳酸钠溶液除去氯气中混有的装置氯化氢,故D错误;
故选C.
点评:本题考查了常见气体的净化、氯气的化学性质,题目难度不大,注意掌握常见气体的化学性质及除杂方法,明确氯气的性质是解答本题的关键.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
某氮肥样品可能含有NH4HCO3、NH4Cl、NH4NO3中的一种或几种.称取该样品0.5000g,溶解配成100.00mL溶液,加过量浓NaOH溶液,加热,将产生的氨气通入60.00mL 0.1000mol?L-1的H2SO4溶液中(设产生的NH3全部逸出),剩余的H2SO4溶液能消耗20.00mL 0.2250mol?L-1的NaOH溶液.下列说法正确的是( )
| A、吸收NH3消耗的H2SO4为6.000×10-3mol |
| B、上述过程共产生NH3 268.8mL |
| C、该样品中NH4+的质量分数为43.2% |
| D、该氮肥样品必含NH4Cl |
电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O═Cl-+Mg(OH)2↓,图②是含Cr2O72-工业废水的电化学处理示意图.下列说法正确的是( )
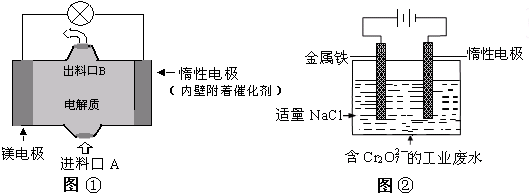

| A、图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| B、图②中阳极上的电极反应式为:Fe-3e-═Fe3+ |
| C、图①中发生的还原反应是:Mg2++ClO-+H2O+2e-═Cl-+Mg (OH)2↓ |
| D、若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀 |
下列类比关系正确的是( )
| A、AlCl3与过量NaOH溶液反应生成[Al(OH)4]-,则与过量NH3?H2O反应也生成[Al(OH)4]- |
| B、Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应 |
| C、Fe与Cl2反应生成FeCl3,则与I2反应可生成FeI3 |
| D、Na2O2与CO2反应生成Na2CO3和O2,则与SO2反应可生成Na2SO3和O2 |
离子方程式H++OH-=H2O可表示的化学方程式是( )
| A、盐酸与氢氧化铜的反应 |
| B、硫酸与氢氧化钠的反应 |
| C、硫酸与氢氧化镁的反应 |
| D、盐酸与氨水的反应 |
氢氧燃料电池是一种污染小,效率高的新型化学电源,可应用于航天器上.其总反应的化学方程式为:2H2+O2=2H2O 该电池的负极反应式为可表示为( )
| A、2H2-4e-=4H+ |
| B、4H++4e-=2H2 |
| C、2H2O+O2+4e-=4OH- |
| D、4OH--4e-=2H2O+O2 |
在25℃时,用蒸馏水稀释1mol/L氨水至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A、
| ||||
B、
| ||||
C、
| ||||
| D、OH-物质的量 |
下列说法正确的是( )
| A、氮原子的质量就是氮的相对原子质量 |
| B、氢氧化钠的摩尔质量是40g |
| C、氩气的摩尔质量在数值上等于它的相对原子质量 |
| D、1mol H2SO4中含有1mol H2 |