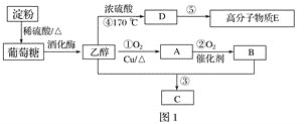
题目内容
【题目】[物质结构与性质]
[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2-+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN

(1)Zn2+基态核外电子排布式为____________________。
(2)1 mol HCHO分子中含有σ键的数目为____________mol。
(3)HOCH2CN分子中碳原子轨道的杂化类型是______________。
(4)与H2O分子互为等电子体的阴离子为________________。
(5)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为_____________。
【答案】(1)1s22s22p62s23p63d10(或[Ar] 3d10)(2)3;(3)sp3和sp;(4)NH2-;
(5) ;
;
【解析】
试题(1)Zn是30号元素,Zn2+核外有28个电子,根据原子核外电子排布规律可知基态Zn2+核外电子排布式为1s22s22p62s23p63d10;
(2)甲醛的结构式是![]() ,在一个甲醛分子中含有3个ρ键和1个π键,所以在1 mol HCHO分子中含有σ键的数目为3 mol;
,在一个甲醛分子中含有3个ρ键和1个π键,所以在1 mol HCHO分子中含有σ键的数目为3 mol;
(3)在HOCH2CN分子中,连有羟基-OH的碳原子的杂化类型是sp3杂化,含有—CN的碳原子轨道的杂化轨道类型是sp杂化;
(4)H2O含有10个电子,则与H2O分子互为等电子体的阴离子为NH2-;
(5)在[Zn(CN)4]2-中Zn2+与CN-的N原子形成配位键,N原子提供一对电子,Zn2+的空轨道接受电子对,则若不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为 。
。

 阅读快车系列答案
阅读快车系列答案【题目】铵盐是比较重要的盐类物质,请回答下列问题:
(1)氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:_________________
(2)实验表明氢氧化镁可溶于氯化铵溶液中,两个观点:氯化铵水解显酸性中和OH-,使氢氧化镁沉淀溶解平衡正移;铵根结合OH-,使氢氧化镁沉淀溶解平衡正移。为了探究反应机理,可向溶液中加入_____盐溶液验证。
(3)NH4SCN溶液与AgNO3溶液反应会生成 AgSCN沉淀。已知:室温下,Ksp(AgCl)=1.8×10-10,Ksp(AgSCN)= 2.0×10-12,则AgCl转化为AgSCN的平衡常数K=____________
(4)常温下向100mL0.2mo/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
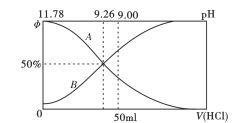
①表示NH3·H2O浓度变化的曲线是__________(填“A”或“B")。
②NH3·H2O的电离常数为__________________(已知lg1.8 = 0.26)。
③当加入盐酸体积为50mL时,溶液中c(NH4+)-c(NH3·H2O) =_____mol/L (用数字表示)。
(5)为了探究外界条件对氯化铵水解平衡的影响,设计如下实验方案:
实验序号 | c(NH4Cl)/mol.L-1 | 温度/℃ | 待测物理量 | 实验目的 |
Ⅰ | 0.5 | 30 | x | - |
Ⅱ | 1.5 | i | y | 探究浓度对氯化铵水解平衡的影响 |
Ⅲ | 0.5 | 35 | z | ii |
Ⅳ | 2.0 | 40 | m | 探究温度、浓度同时对氯化铵水解平衡的影响 |
限选药品和仪器:恒温水浴、pH计、烧杯、0.1mol.L-1硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液.
①实验中,“待测物理量”是_______________
②i=____________________;ii:___________________________________
③上述表格中,y____(填“>”“<”或“=”)m.
【题目】氨基甲酸铵(H2 NCOONH4)是一种易分解、易水解的白色固体。其研究小组以浓氨水、干冰等为原料制备氨基甲酸铵的实验装置如图1所示,其主要反应的原理为2NH3(g)+CO2(g)![]() NH2COONH4(s) △H<0
NH2COONH4(s) △H<0


(1)仪器1的名称是___________。仪器3中盛装的固体是___________,其作用是___________。
(2)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内浓硫酸中产生气泡,则应该___________(填“加快”“减慢”或“不改变”)产生氨气的速率。
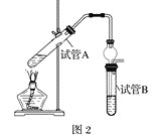
(3)另一种制备氨基甲酸铵的反应装置(液体石蜡和CCl4均充当惰性介质)如图2所示。
①液体石蜡鼓泡瓶的作用是______________________。
②若无冰水,则氨基甲酸铵易分解生成尿素[CO(NH2)2]请写出氨基甲酸铵受热分解的化学方程式:______________________。
③当CCl4液体中产生较多晶体悬浮物时,立即停止反应,过滤分离得到粗产品,为了将所得粗产品干燥,可采取的方法是___________(填标号)。
A.蒸馏 B.真空微热烘干 C.高压加热烘干
(4)制得的氨基甲酸铵中可能含有碳酸氢铵、碳酸铵中的一种或两种杂质(不考虑氨基甲酸铵与水的反应)。
①设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
实验步骤 | 预期现象和结论 |
步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解 | 得到无色溶液 |
步骤2:向试管中加入过量的BaCl2溶液,静置 | 若溶液不变浑浊,则证明固体中不含碳酸铵 |
步骤3:向试管中继续加入___________ | ___________,则证明固体中含有碳酸氢铵 |
②根据①的结论。取15.8g氨基甲酸铵样品,用足量氧氧化钡溶液充分处理后,过滤、洗涤、干燥,测得沉淀质量为1.97g。则样品中氨基甲酸铵的质量分数为___________。
【题目】用50 mL0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液,在如图所示的装置中进行中和反应。测定强酸与强碱反应的反应热。

起始温度t1/℃ | 终止温度 t2/℃ | 温度差 (t2-t1) /℃ | |||
HCl | NaOH | 平均值 | |||
1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
2 | 24.5 | 24.5 | 24.50 | 27.5 | 3.00 |
3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 _________。
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是______________________________。
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指______________温度。
(4)大烧杯上如不盖硬纸板,求得的中和热数值_________(填“偏大”、“偏小”、“无影响”)。
(5)计算该实验发生中和反应时放出的热量为________________kJ(中和后生成的溶液的比热容c=4.18J/(g·℃ ) (保留两位小数)。
(6)如果用50 mL0.55mol/L的氨水(NH3·H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,则△H会_________(填“偏大”、“偏小”、“无影响”),其原因是_________。