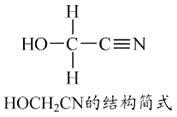
题目内容
【题目】铵盐是比较重要的盐类物质,请回答下列问题:
(1)氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:_________________
(2)实验表明氢氧化镁可溶于氯化铵溶液中,两个观点:氯化铵水解显酸性中和OH-,使氢氧化镁沉淀溶解平衡正移;铵根结合OH-,使氢氧化镁沉淀溶解平衡正移。为了探究反应机理,可向溶液中加入_____盐溶液验证。
(3)NH4SCN溶液与AgNO3溶液反应会生成 AgSCN沉淀。已知:室温下,Ksp(AgCl)=1.8×10-10,Ksp(AgSCN)= 2.0×10-12,则AgCl转化为AgSCN的平衡常数K=____________
(4)常温下向100mL0.2mo/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。

①表示NH3·H2O浓度变化的曲线是__________(填“A”或“B")。
②NH3·H2O的电离常数为__________________(已知lg1.8 = 0.26)。
③当加入盐酸体积为50mL时,溶液中c(NH4+)-c(NH3·H2O) =_____mol/L (用数字表示)。
(5)为了探究外界条件对氯化铵水解平衡的影响,设计如下实验方案:
实验序号 | c(NH4Cl)/mol.L-1 | 温度/℃ | 待测物理量 | 实验目的 |
Ⅰ | 0.5 | 30 | x | - |
Ⅱ | 1.5 | i | y | 探究浓度对氯化铵水解平衡的影响 |
Ⅲ | 0.5 | 35 | z | ii |
Ⅳ | 2.0 | 40 | m | 探究温度、浓度同时对氯化铵水解平衡的影响 |
限选药品和仪器:恒温水浴、pH计、烧杯、0.1mol.L-1硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液.
①实验中,“待测物理量”是_______________
②i=____________________;ii:___________________________________
③上述表格中,y____(填“>”“<”或“=”)m.
【答案】6NH4++Fe2O3=2Fe3++6NH3↑+3H2O或分步写(NH4++H2O![]() NH3·H2O+H+, Fe2O3+6 H+=2Fe3++3H2O) CH3COONH4 90 A 1.8×10-5或10-4.74 2×(10-5-10-9) 溶液的pH 30 探究温度对氯化铵水解平衡的影响 >
NH3·H2O+H+, Fe2O3+6 H+=2Fe3++3H2O) CH3COONH4 90 A 1.8×10-5或10-4.74 2×(10-5-10-9) 溶液的pH 30 探究温度对氯化铵水解平衡的影响 >
【解析】
(1)氯化铵溶液水解显酸性,能溶解氧化铁,离子方程式为:6NH4++Fe2O3==2Fe3++6NH3↑+3H2O或分步写(NH4++H2O![]() NH3·H2O+H+, Fe2O3+6H+=2Fe3++3H2O)。 (2)为了探究反应机理,可以向溶液中加入铵根离子但溶液为中性的盐溶液,CH3COONH4。(3). AgCl转化为AgSCN的平衡常数K=
NH3·H2O+H+, Fe2O3+6H+=2Fe3++3H2O)。 (2)为了探究反应机理,可以向溶液中加入铵根离子但溶液为中性的盐溶液,CH3COONH4。(3). AgCl转化为AgSCN的平衡常数K=![]() 90。(4) ①向氨水中加入盐酸,随着盐酸的量的增加,一水合氨的物质的量减小,所以为曲线A。②氨水的电离平衡常数=
90。(4) ①向氨水中加入盐酸,随着盐酸的量的增加,一水合氨的物质的量减小,所以为曲线A。②氨水的电离平衡常数=![]() ,平衡常数只随温度变化,取曲线的交点,即pH=9.26,此时铵根离子浓度和一水合氨浓度相等,c(OH-)=
,平衡常数只随温度变化,取曲线的交点,即pH=9.26,此时铵根离子浓度和一水合氨浓度相等,c(OH-)= ![]() ,则有K= 1.8×10-5或10-4.74。③当加入盐酸的体积为50mL时,此时溶液的pH为9,溶液中存在等浓度的一水合氨和氯化铵,溶液中存在电荷守恒c(NH4+)+ c(H+)=c(OH-)+ c(Cl-),物料守恒c(NH4+)+c(NH3·H2O)= 2c(Cl-),得到c(NH4+) -c(NH3·H2O)= 2c(OH-)-2 c(H+)=2×(10-5-10-9)mol/L。(5)①由提供的药品和仪器可知,pH计是准确测定溶液的pH的,所以待测物理量是溶液的pH。②探究浓度对氯化铵水解平衡的影响,则温度必须相同,所以实验Ⅱ的温度与实验Ⅰ相同,即为30度。实验Ⅰ和实验Ⅲ浓度相同,温度不同,所以是探究温度对氯化铵水解平衡的影响。③水解反应属于吸热反应,温度越高水解程度越大,氢离子浓度增大,浓度越高,水解生成的氢离子浓度越大,则溶液的酸性越强,已知实验Ⅳ的浓度大,温度高,所以溶液的pH小,即y>m。
,则有K= 1.8×10-5或10-4.74。③当加入盐酸的体积为50mL时,此时溶液的pH为9,溶液中存在等浓度的一水合氨和氯化铵,溶液中存在电荷守恒c(NH4+)+ c(H+)=c(OH-)+ c(Cl-),物料守恒c(NH4+)+c(NH3·H2O)= 2c(Cl-),得到c(NH4+) -c(NH3·H2O)= 2c(OH-)-2 c(H+)=2×(10-5-10-9)mol/L。(5)①由提供的药品和仪器可知,pH计是准确测定溶液的pH的,所以待测物理量是溶液的pH。②探究浓度对氯化铵水解平衡的影响,则温度必须相同,所以实验Ⅱ的温度与实验Ⅰ相同,即为30度。实验Ⅰ和实验Ⅲ浓度相同,温度不同,所以是探究温度对氯化铵水解平衡的影响。③水解反应属于吸热反应,温度越高水解程度越大,氢离子浓度增大,浓度越高,水解生成的氢离子浓度越大,则溶液的酸性越强,已知实验Ⅳ的浓度大,温度高,所以溶液的pH小,即y>m。

 阅读快车系列答案
阅读快车系列答案【题目】常温下,1mol化学键断裂形成气态原子所需要的能量用![]() 表示。结合表中信息判断下列说法不正确的是( )
表示。结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. 表中最稳定的共价键是H-F键
C. H2(g)→2H(g) △H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) △H=-25kJ/mol