题目内容
【题目】下列叙述与图象对应符合的是
A.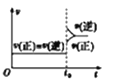 对于达到平衡状态的
对于达到平衡状态的![]()
![]() 在t0时刻充入了一定量的
在t0时刻充入了一定量的![]() ,平衡逆向移动
,平衡逆向移动
B. 对于反应
对于反应![]() ,
,![]() ,
,![]()
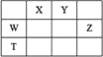
C.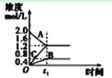 该图象表示的化学方程式为:
该图象表示的化学方程式为:![]()
D. 对于反应
对于反应![]() ,y可以表示Y的百分含量
,y可以表示Y的百分含量
【答案】B
【解析】
A.对于达到平衡状态的N2(g)+3H2(g)2NH3(g)在t0时刻充入了一定量的NH3,c(NH3)立即增大,故V逆立即增大,由于反应物的浓度是在原来基础上逐渐增大,故V正在原来基础上逐渐增大,不会出现突变,故A错误;
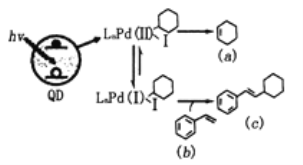
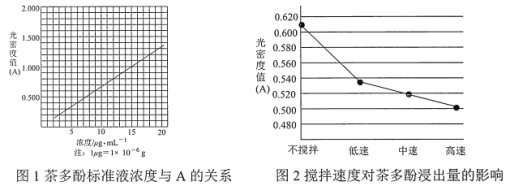
B.根据“定一议二”的原则,将曲线a和b做对比可知压强p2>p1,将曲线b和c做对比可知温度T1>T2,故B正确;
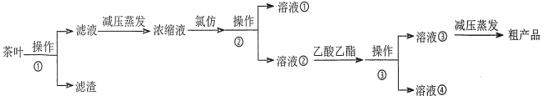
C.根据图象可知,A为反应物,B和C为生成物,在t1时反应达平衡,A、B、C的浓度该变量分别为0.8mol/L、0.4mol/L和1.2mol/L,故A、B、C的计量数之比为2∶1∶3,由于此反应最后达平衡,故为可逆反应,故化学方程式为:2AB+3C,故C错误;
D.从图象可知,温度T升高,y降低。而对于反应2X(g)+3Y(g)2Z(g)△H<0,升高温度,平衡左移,Y的百分含量升高,故y不能表示Y的百分含量,故D错误;
故选B。

练习册系列答案
相关题目
【题目】常温下浓度均为0.1mol/L 的四种盐溶液,其pH 如表所示,下列说法正确的是( )
序号 | ① | ② | ③ | ④ |
溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
pH | 8.8 | 9.7 | 11.6 | 10.3 |
A. 将等浓度的CH3COOH 和HClO溶液,pH小的是HClO
B. Na2CO3和NaHCO3溶液中粒子种类不同
C. 溶液水的电离程度:①>②>④>③
D. NaHCO3溶液中:c (Na+) =c (CO32- )+c (HCO3- )+c (H2CO3)