��Ŀ����
7����1����̬��ԭ�ӵļ۵����Ų�ʽΪ3d54s1����2��CrO2Cl2��NaClO�������������������������Ȼ������Ʊ�CrO2Cl2�ķ�ӦΪ��K2Cr2O7+3CCl4�T2KCl+2CrO2Cl2+3COCl2����������Ӧʽ�зǽ���Ԫ�ص縺���ɴ�С��˳����O��Cl��C����Ԫ�ط��ű�ʾ����
��3����������������������ߣ����ڵĻ�����ȫ��ʳƷ��ȫԽ��ԽΪ��������ע����ȩ��HCHO����������Ҫ������Ⱦ��֮һ����е���-19.5�棩���״���CH3OH���ǡ��پơ��е���Ҫ�к����ʣ���е���64.65�棩���״��ķе����Ը��ڼ�ȩ����Ҫԭ���Ǽ״����Ӽ�������������ȩ���Ӽ䲻�������
��4��˫�谷�ṹ��ʽ��ͼ1��ʾ��
��˫�谷�����ЦҼ��ͦм���Ŀ֮��Ϊ3��1��
��˫�谷����̼ԭ�ӵ��ӻ�����Ϊsp��sp2��
��5����Ԫ�����γɶ�������������[Ni��CN��4]2+�в����е���������AE����ѡ���ţ���
A�����Ӽ� B����λ�� C���� D���� E�����
��6��������Ա�о�����������Ϊ�缫�Ĺ⻯ѧ��أ������������������ȵ缫��ʹˮ�ֽ������������֪�����Ⱦ����ṹ��ͼ2��ʾ�����仯ѧʽΪSrTiO3��

���� ��1�����ݺ�������Ų����ɿ���д���۵����Ų�ʽ��
��2����Ӧʽ�зǽ���Ԫ�������֣�O��C��Cl����ϻ�����CCl4��NaClO��Ԫ�ػ��ϼ��жϣ�
��3�����ݼ״����Ӽ����������۷е�����
��4���ٵ���Ϊ�Ҽ��ͣ�˫������1���Ҽ���1���м�������������1���Ҽ���2���м���
��ԭ���ӻ������Ŀ=�Ҽ���+�µ��Ӷԣ���Ͻṹ��ʽȷ��Cԭ���ӻ������Ŀ������ȷ�����ӻ���ʽ��
��5��̼����Ϊ��������������1���Ҽ���2���м���������Ϊ��λ����
��6�����ݾ�̯�����㾧����Sr��Ti��Oԭ����Ŀ������ȷ����ѧʽ��
��� �⣺��1�����ݺ�������Ų����ɿ���д����̬���۵����Ų�ʽΪ1s22s22p63s23p63s23p63d54s1�����Ի�̬����Cr��ԭ�ӵļ۵����Ų�ʽ��3d54s1��
�ʴ�Ϊ��3d54s1��
��2����Ӧʽ�зǽ���Ԫ�������֣�O��C��Cl��CCl4��C���������ϼۡ�Cl���ָ����ϼۣ�NaClO��ClΪ+1�ۣ�OΪ-2�ۣ��縺��Խ�Լ��ϵ���������Խ��Ԫ�������ʱ��Ԫ�ر��ָ��ۣ��ʵ縺�ԣ�O��Cl��C��
�ʴ�Ϊ��O��Cl��C��
��3���״����Ӽ����������۷е�������ȩ���Ӽ䲻����������ʼ״��ķе�ϸߣ�
�ʴ�Ϊ���״����Ӽ�������������ȩ���Ӽ䲻���������
��4���ٵ���Ϊ�Ҽ��ͣ�˫������1���Ҽ���1���м�������������1���Ҽ���2���м���˫�谷������9���Ҽ�����3���м���˫�谷�����ЦҼ��ͦм���Ŀ֮��Ϊ9��3=3��1��
�ʴ�Ϊ��3��1��
��-C��N��Cԭ���γ�2���Ҽ������Ӱ�����Cԭ�ӳ�3���Ҽ�����û�йµ��Ӷԣ�Cԭ���ӻ������ֱ�Ϊsp��sp2��
�ʴ�Ϊ��sp��sp2��
��5��������[Ni��CN��4]2-����1���Ҽ���2���м���������Ϊ��λ�������������Ӽ��������
��ѡ��AE��
��6���ɾ����ṹ��֪��������Srԭ����ĿΪ8��$\frac{1}{8}$=1��Tiԭ����ĿΪ1����ԭ���γ���������ṹ��Oԭ����ĿΪ6��$\frac{1}{2}$=3���ʸ����ʻ�ѧʽΪ��SrTiO3��
�ʴ�Ϊ��SrTiO3��
���� ���⿼�����ʵĽṹ�����ʣ��漰�����Ų�ʽ���縺�ԡ��ӻ��������ѧ���ȣ�֪ʶ��϶࣬��Ŀ�ۺ��Խ�ǿ���ѶȽϴ�

 һ����������ϵ�д�
һ����������ϵ�д�| A�� | �����Ũ�Ȳ��ٱ仯 | B�� | ������ѹǿ���ٸı� | ||
| C�� | ����ķ��������ٱ仯 | D�� | �������Ũ����� |
| A�� | ��������ƽ��ȡ3.25gNaCl | |
| B�� | ����Ͳ��ȡ10.51mL���� | |
| C�� | ����ʽ�ζ�����ȡ20.00mLKMnO4��Һ | |
| D�� | ������ƿ����216mL0.1mol/L��NaOH��Һ |
| A�� | ͬŨ��������Һ�У��٣�NH4��2SO4 ��NH4HCO3 ��NH4Cl����NH3•H2O��c��NH4+���ɴ�С��˳���ǣ��٣��ۣ��ڣ��� | |
| B�� | ����ʱ���������������Ͱ�ˮ��Ϻ�pH=7����c ��NH4+����c ��Cl-�� | |
| C�� | 0.2 mol•L-1Na2CO3��Һ�У�c ��CO32-��+c ��HCO3-��+c ��H2CO3��=0.2 mol•L-1 | |
| D�� | ���������Һ�м����������ᣬ�õ�������Һ��c��Na+����c��CH3COO-����c��H+����c��OH-�� |
| A�� | 1��1 | B�� | 2��1 | C�� | 1��2 | D�� | 4��1 |
 ��1���������������ɺ����ʿɽ������·��ࣺ
��1���������������ɺ����ʿɽ������·��ࣺ ��������Ȼ�̼��Һ��Ӧ��1��1���IJ���Ľṹ��ʽ��
��������Ȼ�̼��Һ��Ӧ��1��1���IJ���Ľṹ��ʽ��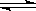 CH4(g��+nH2O(l����Q(Q��0������ܹ����ڿ�ȼ��������Ϊ��������������е�( ��
CH4(g��+nH2O(l����Q(Q��0������ܹ����ڿ�ȼ��������Ϊ��������������е�( ��