题目内容
18.无法判断可逆反应2SO2(g)+O2(g)?2SO3(g)是否达到平衡的理由是( )| A. | 气体的浓度不再变化 | B. | 容器内压强不再改变 | ||
| C. | 气体的分子数不再变化 | D. | 各气体的浓度相等 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、反应混合物中各物质的浓度不再改变,说明正逆反应速率相等,故A不选;
B、此反应为前后气体体积不相等的反应,容器内压强不再改变,说明反应达到平衡,故B不选;
C、气体的分子数不再变化,说明气体的物质的量不再改变,说明反应达到平衡,故C不选;
D、各种气体的浓度相等,不能说明正逆反应的状态,不能判断是否平衡,故D选,故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列说法中正确的是( )
| A. | 凡是放热反应都是自发的,吸热反应都是非自发的 | |
| B. | 自发反应一定是熵增大,非自发反应一定是熵减小或不变 | |
| C. | 醋酸溶液的导电能力可能比稀硫酸强 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
13.在水中加入下列物质,能促进水的电离且溶液为碱性的是( )
| A. | H2SO4 | B. | NH4Cl | C. | CH3COONa | D. | NaOH |
10.下列物质加入水中,能使水的电离度增大且溶液显酸性的是( )
| A. | Al2(SO4)3 | B. | HCl | C. | Na2S | D. | NH3.H2O |
 和
和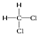
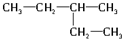 和
和