题目内容
1.已知:CH3(CH2)2CH3(g)+$\frac{13}{2}$O2(g)═4CO2(g)+5H2O(l);△H=-2878kJ•mol-1(CH3)2CHCH3(g)+$\frac{13}{2}$O2(g)═4CO2(g)+5H2O(l);△H=-2869kJ•mol-1
下列说法正确的是( )
| A. | 正丁烷的燃烧热为-2878kJ•mol-1 | |
| B. | 正丁烷分子所具有的能量大于异丁烷分子 | |
| C. | 等量的异丁烷分子中碳氢键比正丁烷的多 | |
| D. | 异丁烷转化为正丁烷的过程是一个放热过程 |
分析 A、燃烧热是1mol物质完全燃烧生成稳定氧化物放出热量,根据题给热化学方程式分析判断;
B、热化学方程式相减得到CH3CH2CH2CH3(g)═(CH3)2CHCH3(g)△H=-9kJ•mol-1,说明反应物质的总能量大于生成物的总能量;
C、根据烷烃的结构特征分析解决,烷烃分子中碳原子都是以单键和其他原子连接;
D、由题给热化学方程式两式相减得到异丁烷转化为正丁烷的热化学方程式即可做出判断.
解答 解:A、燃烧热是1mol物质完全燃烧生成稳定氧化物放出热量,热化学方程式是两种可燃物质的燃烧热,正丁烷的燃烧热△H=-2878kJ•mol-1,故A正确;
B、热化学方程式相减得到CH3CH2CH2CH3(g)═(CH3)2CHCH3(g)△H=-9kJ•mol-1,此过程是一个放热过程,所以正丁烷能量高于异丁烷,故B正确;
C、等量的正丁烷和异丁烷是同分异构体,都是烷烃,烷烃中碳原子形成的化学键都是单键,所以分子内有多少个氢原子,就会有多少个碳氢键,所以二者所含碳氢键相同,故C错误;
D、热化学方程式相减得到(CH3)2CHCH3(g)═CH3CH2CH2CH3(g)△H=+9kJ•mol-1,异丁烷转化为正丁烷的过程是一个吸热过程,故D错误;
故选:AB.
点评 本题考查了热化学方程式的应用,物质的能量高低比较,有机物分子结构的判断等知识.

练习册系列答案
相关题目
9.下列有关盐酸、硝酸、硫酸的叙述正确的是( )
| A. | 都是无色液体 | B. | 都是易挥发有刺激性气味的液体 | ||
| C. | 浓溶液在空气中都有白雾生成 | D. | 都是易溶于水的强酸 |
16.设NA为阿伏伽德罗常数的数值,下列叙述不正确的是( )
| A. | 标准状况下,4.4g CO2中含有的原子数为0.3NA | |
| B. | 标准状况下,22.4L甲烷中含有的C-H键数为4NA | |
| C. | 5.6g 铁粉与硝酸反应失去的电子数可能为0.25NA | |
| D. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1 mol•L-1 |
5.下列实验能到达预期目的是( )
| 实验内容 | 实验目的 | |
| A | 测定同浓度的Na3PO4和Na2SO4水溶液的pH | 探究磷、硫两种元素非金属性的强弱 |
| B | 向蔗糖溶液中加入4滴稀硫酸,煮沸几分钟,冷却,再加入银氨溶液,水溶加热 | 检验蔗糖是否已水解 |
| C | 将乙醇与浓硫酸共热产生气体直接通入酸性kMnO4溶液 | 检验乙烯的生成 |
| D | 向AgCl沉淀中滴加少量KI溶液,观察白色沉淀转化为黄色沉淀 | 验证Ksρ(AgCl)>Ksρ(AgI) |
| A. | A | B. | B | C. | C | D. | D |
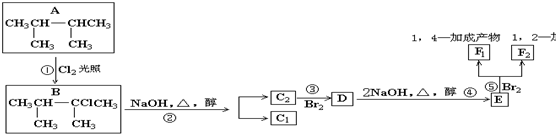
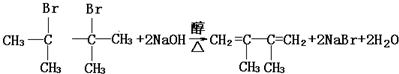 ;
;