题目内容
7. 硼是新型无机材料中的明星元索.
硼是新型无机材料中的明星元索.(l)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为BBr3+PBr3+3H2$\frac{\underline{\;高温\;}}{\;}$BP+6HBr,图为磷化硼晶体结构中最小的重复单元.磷化硼的晶体类型是原子晶体,一个晶胞中含4个P原子.每个B或P均形成4个共价键,其中有一个配位键,提供空轨道的是B原于.
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是N(填元素符号),其基态原子的电子排布式为1s22s22p3,氮化硼中B元索的化合价为+3.
(3)环硼氮烷与苯是等电子体.其一氯代物有两种结构、二氯代物有四种结构.写出环硼氮烷分子结构式
 .
.(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料.在BF3 分子中,F-B-F的键角是120度,B原子采用sp2杂化; BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为正四面体.
分析 (1)反应物是三溴化硼、三溴化磷和氢气,反应条件是高温,生成物是BP,根据元素守恒知还生成HBr,根据反应物、生成物及反应条件书写方程式;原子晶体的构成微粒是原子,为空间网状结构;根据图知,该晶胞中P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,P原子含有孤电子对、B原子含有空轨道;
(2)同一周期元素,元素电负性随着原子序数增大而增大;N原子核外有7个电子,根据构造原理书写其基态原子核外电子排布式;氮化硼中N元素化合价为-3价,则B元素化合价为+3价;
(3)环硼氮烷与苯是等电子体.根据苯的结构写出BN的大致结构,再根据一氯代物、二氯代物结构确定N、B原子在环上交叉出现,从而确定其结构简式;
(4)在BF3 分子中,B原子价层电子对个数为3且不含孤电子对,所以为平面正三角形结构,据此计算F-B-F的键角及原子杂化方式,BF4-中B原子价层电子对个数是4且不含孤电子对,其空间构型是正四面体.
解答 解:(1)反应物是三溴化硼、三溴化磷和氢气,反应条件是高温,生成物是BP,根据元素守恒知还生成HBr,根据反应物、生成物及反应条件书写方程式为BBr3+PBr3+3H2$\frac{\underline{\;高温\;}}{\;}$BP+6HBr;原子晶体的构成微粒是原子,为空间网状结构,所以BP是原子晶体;根据图知,该晶胞中P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,P原子含有孤电子对、B原子含有空轨道,所以提供空轨道的原子是B原子,
故答案为:BBr3+PBr3+3H2$\frac{\underline{\;高温\;}}{\;}$BP+6HBr;原子晶体;4;B;
(2)同一周期元素,元素电负性随着原子序数增大而增大,所以N元素电负性较大;N原子核外有7个电子,根据构造原理书写其基态原子核外电子排布式为1s22s22p3;氮化硼中N元素化合价为-3价,则B元素化合价为+3价,
故答案为:N;1s22s22p3;+3;
(3)环硼氮烷与苯是等电子体.根据苯的结构写出BN的大致结构,再根据一氯代物、二氯代物结构确定N、B原子在环上交叉出现,从而确定其结构简式为 ,故答案为:
,故答案为: ;
;
(4)在BF3 分子中,B原子价层电子对个数为3且不含孤电子对,所以为平面正三角形结构,所以F-B-F的键角为120度,原子杂化方式为sp2,BF4-中B原子价层电子对个数是4且不含孤电子对,其空间构型是正四面体,故答案为:120;sp2;正四面体.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、原子杂化方式判断、微粒空间构型判断、原子核外电子排布等知识点,利用均摊法、价层电子对互斥理论、构造原理分析解答即可,难点是(3)题结构简式判断.

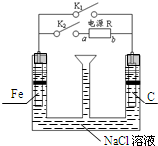
| A. | 若只关闭K1,则Fe发生析氢腐蚀 | |
| B. | 先只关闭K1,漏斗内液面下降,且有红褐色沉淀产生;再打开K1,仅关闭K2,则液面上升 | |
| C. | 若只关闭K2,只有一个电极产生气体,则a为电源负极 | |
| D. | 只关闭K1时,发生的总反应方程式为:2Fe+O2+2H2O═2Fe(OH)2 |
| A. | 如果某化合物只含共价键,则其一定是共价化合物 | |
| B. | 焓变小于0而熵变大于0的反应肯定是自发反应 | |
| C. | 对于给定条件下反应物之间同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 绿色化学的核心是利用化学原理对产生的环境污染进行治理 |
| 弱酸化学式 | HX | HY | H2CO3 |
| 电离平衡常数 | 7.8×10-9 | 3.7×10-15 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | HX、HY两种弱酸的酸性:HX<HY | |
| B. | 相同条件下溶液的碱性:NaX>Na2CO3>NaY>NaHCO3 | |
| C. | 结合H+的能力:CO32->Y->X->HCO3- | |
| D. | HX与Na2CO3反应,无气泡产生 |
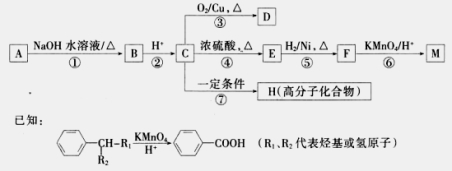

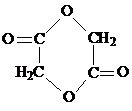 .
. .写出反应 ②的化学方程式
.写出反应 ②的化学方程式 .
. ,属于分子晶体(填晶体类型).
,属于分子晶体(填晶体类型).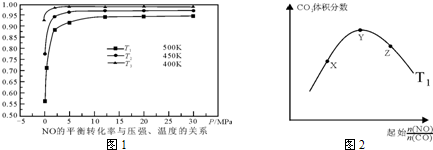
 Fe2O3+2Al
Fe2O3+2Al