题目内容
以地下卤水(主要含NaCl,还有少量Ca2+、Mg2+)为主要原料生产亚硫酸钠的新工艺如下,同时能得到用作化肥的副产品氯化铵。
已知以下四种物质的溶解度曲线图:
(1)“除杂”时,先加入适量石灰乳过滤除去Mg2+,再通入CO2并用少量氨水调节pH过滤除去Ca2+,“废渣”的主要成分为 、 。
(2)“滤渣1”的化学式为 。
(3)在“滤液1”中加入盐酸的目的是 。“滤渣2”的化学式为 。
(4)已知H2CO3和H2SO3的电离常数如下表,“通入SO2”反应的化学方程式为 。
| 物质 | 电离常数(25℃) |
| H2CO3 | K1=4.4X10-7 K2=4.7X10-11 |
| H2SO3 | K1=1.23X10-2 K2=5.6X10-8 |
(16分)(1)Mg (OH)2(2分) CaCO3(2分)
(2)NaHCO3(3分)
(3)除去HCO3-(3分,多答“使更多的Na+形成NaCl析出,提高NH4Cl的纯度”不扣分) NaCl(3分)
(4)NaHCO3+SO2 = NaHSO3+ CO2(3分)
解析试题分析:(1)依题意,除杂步骤涉及的反应为Ca(OH)2+Mg2+=Mg(OH)2+Ca2+,CO2+2NH3?H2O=2NH4++CO32-+H2O,Ca2++CO32-=CaCO3↓,则废渣的主要成分是Mg(OH)2、CaCO3;(2)由溶解度曲线可知,NaHCO3的溶解度最小,最先达到饱和,则NH4HCO3与饱和NaCl具备发生复分解反应发生的条件,即NH4HCO3+NaCl=NaHCO3↓+NH4Cl,因此滤渣1的主要成分是NaHCO3;(3)过滤后滤液1中的主要成分是NaCl、NH4Cl、NaHCO3,氯化纳和氯化铵都不能与盐酸反应,而碳酸氢钠与盐酸能反应,即HCO3-+H+=CO2↑+H2O,因此加入足量盐酸能除去HCO3-,提高NH4Cl的纯度;由溶解度曲线可知,热溶液中NaCl的溶解度小于NH4Cl,因此蒸发浓缩、趁热过滤得到的滤渣2为NaCl,而滤液则含有NH4Cl、NaCl;由于NH4Cl的溶解度随温度降低明显减小,而NaCl的溶解度随温度降低无明显变化,则蒸发浓缩、冷却结晶可制备NH4Cl晶体;(4)滤渣1为NaHCO3,根据表中的电离常数可知电离程度:H2SO3>H2CO3>HSO3->HCO3-,根据复分解反应发生的条件可知,通入SO2的反应为NaHCO3+SO2=NaHSO3+CO2,不可能为2NaHCO3+SO2=Na2SO3+2CO2+H2O,因为CO2+H2O+Na2SO3= NaHSO3+NaHCO3。
考点:考查化学工艺流程大题,涉及除杂原理、分离提纯的方法、滤渣组成、化学方程式等的推断。

在H2SO4、HNO3、NH3的工业生产中,具有的共同点是
| A.使用H2作原料 | B.使用催化剂 |
| C.使用吸收塔设备 | D.使用尾气吸收装置 |
合成氨工业上采用循环操作的原因主要是( )
| A.加快反应速率 |
| B.能提高NH3的平衡浓度 |
| C.降低NH3的沸点 |
| D.提高N2和H2的利用率 |
下列关于合成氨工业的叙述可用勒夏特列原理来解释的是 ( )。
| A.使用铁触媒,使平衡向生成NH3的方向移动 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.500 ℃左右比室温更有利于合成氨的反应 |
| D.合成氨时采用循环操作可提高原料的利用率 |
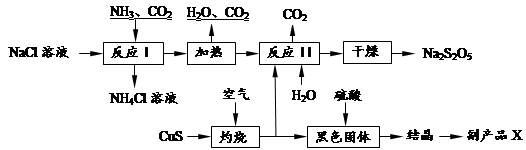
 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。
 2H2(g)+S2(g),其平衡常数表达式为K=。
2H2(g)+S2(g),其平衡常数表达式为K=。
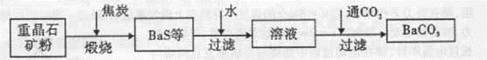
 BaCO3(s)+SO42-(aq)
BaCO3(s)+SO42-(aq)