题目内容
11.下列说法错误的是( )| A. | 化学反应速率越快,反应现象越明显 | |
| B. | 需要加热才能进行的化学反应不一定是吸热反应 | |
| C. | 仅由非金属元素组成的化合物中可能含离子键 | |
| D. | ⅠA族金属元素是同周期中金属性最强的元素 |
分析 A.如无明显反应现象,则无论反应快慢,都不能判断;
B.反应是否吸热与反应条件无关;
C.铵盐由非金属元素组成,为离子化合物;
D.同周期元素从左到右,金属性逐渐减弱.
解答 解:A.化学反应速率越快,反应现象不一定越明显,如中和反应,故A错误;
B.反应是否吸热与反应条件无关,如铝热反应为放热反应,但需在高温下反应,故B正确;
C.铵盐由非金属元素组成,为离子化合物,含有离子键,故C正确;
D.同周期元素从左到右,金属性逐渐减弱,所以ⅠA族金属元素是同周期中金属性最强的元素,故D正确.
故选A.
点评 本题考查较为综合,涉及化学反应与能量、化学反应速率、离子键以及元素周期率知识,为高考常见题型和高频考点,侧重于双基的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
17.X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和.下列叙述正确的是( )
| A. | R的最高价氧化物对应的水化物的酸性比X的弱 | |
| B. | 非金属性:Y>X | |
| C. | 原子半径的大小顺序:X>Z | |
| D. | Z元素最高价氧化物对应的水化物具有两性 |
19.下列说法中不正确的是( )
| A. | 离子化合物中不一定含有金属元素 | |
| B. | 由不同原子所形成的纯净物不一定是化合物 | |
| C. | 分子中一定含有化学键 | |
| D. | 含有金属元素的离子不一定是阳离子 |
6.在下列溶液中,各组离子一定能够大量共存的是( )
| A. | Cu2+、Mg2+、SO42- | B. | H+、Mg2+、CO32- | C. | Ag+、NO3-、Cl- | D. | Fe2+、H+、NO3- |
16.下列说法可以证明反应N2(g)+3H2(g)?2NH3(g)已达到平衡状态的是( )
| A. | 1个N≡N键断裂的同时,有3个H-H键形成 | |
| B. | 1个N≡N键断裂的同时,有3个H-H键断裂 | |
| C. | N2、H2、NH3的分子数之比为1:3:2 | |
| D. | 1个N≡N键断裂的同时,有6个H-N键形成 |
 D
D
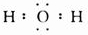
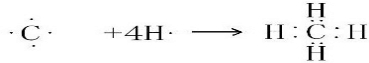 .
.