题目内容
下列指定溶液中,各组离子可能大量共存的是( )
| A、pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
| B、在强酸溶液中:Na+、ClO-、Cl-、Ba2+ |
| C、在含有大量Fe3+的溶液中:NH4+、Cl-、Na+、SCN- |
| D、由水电离的c(H+)=10-13mol?L-1的溶液中:Mg2+、Cl-、K+、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.pH=1的溶液呈酸性,发生氧化还原反应的离子不能大量共存;
B.强酸溶液中,弱酸的酸根离子不能大量共存;
C.与Fe3+反应的离子不能大量共存;
D.由水电离的c(H+)=10-13mol?L-1的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性.
B.强酸溶液中,弱酸的酸根离子不能大量共存;
C.与Fe3+反应的离子不能大量共存;
D.由水电离的c(H+)=10-13mol?L-1的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性.
解答:
解:A.pH=1的溶液呈酸性,Fe2+、NO3-发生氧化还原反应而不能大量共存,故A错误;
B.强酸溶液中,ClO-不能大量共存,且ClO-与Cl-发生氧化还原反应,故B错误;
C.SCN-与Fe3+发生络合反应而不能大量共存,故C错误;
D.由水电离的c(H+)=10-13mol?L-1的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,酸性条件下离子之间不发生任何反应,可大量共存,故D正确.
故选D.
B.强酸溶液中,ClO-不能大量共存,且ClO-与Cl-发生氧化还原反应,故B错误;
C.SCN-与Fe3+发生络合反应而不能大量共存,故C错误;
D.由水电离的c(H+)=10-13mol?L-1的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,酸性条件下离子之间不发生任何反应,可大量共存,故D正确.
故选D.
点评:本题考查离子共存问题,为高频考点,综合考查元素化合物知识,侧重于考查学生化学知识的综合运用,易错点为A,注意发生氧化还原反应的性质,题目难度不大.

练习册系列答案
相关题目
下列电离方程式中正确的是( )
| A、H2SO4=H2++SO42- |
| B、NaHCO3=Na++H++CO32- |
| C、Ca(OH)2=Ca2++2OH- |
| D、CaCl2=Ca+2+2Cl- |
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )| A、该电池工作时电能转化为化学能 |
| B、该电池中电极a是正极 |
| C、该电池的总反应:2H2+O2═2H2O |
| D、外电路中电子由电极b通过导线流向电极a |
关于苯的下列说法正确的是( )
| A、苯的分子是环状结构,其性质跟环烷烃相似 |
B、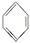 表示苯的分子结构,其中含有碳碳双键,因此苯的性质跟烯烃相同 表示苯的分子结构,其中含有碳碳双键,因此苯的性质跟烯烃相同 |
| C、苯的分子式是C6H6,分子中的C原子远没有饱和,因此能使溴水褪色 |
| D、苯环上的碳碳键的键能、键长介于单双键之间 |
下列反应离子方程式表示不正确的是( )
| A、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
| B、Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C、向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| D、向次氯酸钠溶液中通入少量SO2:ClO-+SO2+H2O=Cl-+SO42-+2H+ |
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、标准状况下,22.4L Cl2完全溶于水时,转移电子数为NA |
| B、常温下,pH=1的H2SO4溶液中含有的H+的数目为0.1NA |
| C、标准状况下,2.24L SO3中含有硫原子的数目为NA |
| D、常温下,23g NO2和N2O4的混合气体中含有NA个氧原子 |
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、T℃时,1 L pH=6纯水中,约含6.02×1017个OH- |
| B、6.8g熔融的KHSO4中含有6.02×1022个阳离子 |
| C、Na2O2与H2O反应,生成常温常压下16g O2,反应中转移电子数为2NA |
| D、用含有0.1mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒个数等于0.1NA |
举世闻名的秦兵马俑制品的主要材料在成分上属于( )
| A、氧化铝 | B、二氧化硅 |
| C、硅酸盐 | D、合金 |
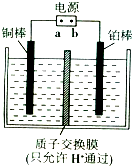 工业上将烟气中的二氧化硫转化为硫,常用的两种方法分别是热解气还原法和离子膜电解法.
工业上将烟气中的二氧化硫转化为硫,常用的两种方法分别是热解气还原法和离子膜电解法.