题目内容
12.9.5gMgCl2固体溶于水配成500mL溶液,其浓度为0.2mol•L-1,从中取出100mL溶液,其中Cl-的浓度为0.4mol•L-1.分析 根据n=$\frac{m}{M}$计算氯化镁物质的量,再根据c=$\frac{n}{V}$计算溶液物质的量浓度,溶液是均一的,取出溶液中氯离子浓度等于原溶液中氯离子浓度.
解答 解:9.5gMgCl2的物质的量为$\frac{9.5g}{95g/mol}$=0.1mol,溶于水配成500mL溶液,其浓度为$\frac{0.1mol}{0.5L}$=0.2mol/L,溶液是均一的,取出溶液中氯离子浓度等于原溶液中氯离子浓度,从中取出100mL溶液,其中Cl-的浓度为2×0.2mol/L=0.4mol/L,
故答案为:0.2;0.4.
点评 本题考查物质的量浓度计算,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
3.下列说法正确的是( )
| A. | 在101kPa时,1mol C与适量O2反应生成1mol CO时,放出110.5kJ热量,则C的燃烧热为110.5kJ/mol | |
| B. | 在10lkPa时lmol H2完全燃烧生成液态水放出285.8kJ热量,H2燃烧热为-285.8KJ/mol | |
| C. | 鉴定HCl和NaOH反应的中和热时,每次实验均应测量3个温度即盐酸起始温度、NaOH起始温度和反应后终止温度 | |
| D. | 在稀溶液中:H+(aq)+oH-(aq)═H2O(l)△H=-57.3KJ/mol,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3KJ |
7.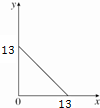 某温度(T℃)下的溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图所示,请回答下列问题:
某温度(T℃)下的溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图所示,请回答下列问题:
(1)该温度T>25℃(填“>”、“<”或“=”).
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示.
假设溶液混合前后的体积变化忽略不计,则a=4,实验②中b=8.
(3)在此温度下,将10mL 0.1mol•L-1的Ba(OH)2溶液分别与5mL 0.1mol•L-1的NaHSO4溶液混合,所得溶液的pH为12.如果将等浓度等体积的Ba(OH)2溶液与NH4Cl溶液混合,所得溶液中各离子浓度由大到小的排列顺序是c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+).
 某温度(T℃)下的溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图所示,请回答下列问题:
某温度(T℃)下的溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图所示,请回答下列问题:(1)该温度T>25℃(填“>”、“<”或“=”).
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示.
| 实验 序号 | Ba(OH)2溶液 的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 9 |
| ② | 22.00 | 18.00 | b |
| ③ | 22.00 | 22.00 | 6 |
(3)在此温度下,将10mL 0.1mol•L-1的Ba(OH)2溶液分别与5mL 0.1mol•L-1的NaHSO4溶液混合,所得溶液的pH为12.如果将等浓度等体积的Ba(OH)2溶液与NH4Cl溶液混合,所得溶液中各离子浓度由大到小的排列顺序是c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+).
4.在500mL 2mol/L KAl(SO4)2的明矾溶液中滴入含有1.5mol溶质的Ba(OH)2溶液,充分反应后铝元素的存在形式是( )
| A. | Al(OH)3和Al3+ | B. | Al(OH)3 | ||
| C. | Al3+、Al(OH)3 和AlO2- | D. | 全部为AlO2- |
1.用36.5%的浓盐酸(密度为1.20g.•mL-1)配制0.2mol•L-1的稀盐酸,引起所配溶液浓度偏高的操作是( )
| A. | 容量瓶实验前用蒸馏水洗干净,但未烘干 | |
| B. | 定容观察液面时俯视 | |
| C. | 用量筒量取一定量液体时,俯视液面读数 | |
| D. | 加蒸馏水时不慎超过了刻度 |
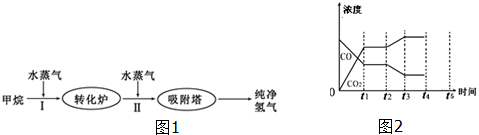
2.工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图1:
(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),反应的平衡常数随温度的变化如表:
从表可以推断:此反应是放(填“吸”或“放”)热反应.400℃时,H2浓度为2mol/L,CO2浓度为1.5mol/L,H2O浓度为3mol/L,CO浓度为1mol/L,则下一时刻,反应向正向(填”正向”或”逆向”)进行.
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第Ⅱ步反应,达到平衡后下列关系正确的是AD.
A.2c1=c2=c3 B.2Q1=Q2=Q3 C.α1=α2=α3 D.α1+α2=1
(3)在一个绝热等容容器中,不能判断此流程的第Ⅱ步反应达到平衡的是②③.
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
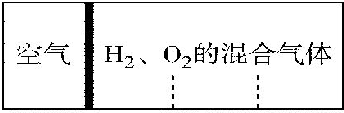
(4)如图2表示此流程的第Ⅱ步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是降低温度、增加水蒸汽的量(或减少氢气的量)(写出两种).若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变).
(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第Ⅱ步反应,达到平衡后下列关系正确的是AD.
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
(3)在一个绝热等容容器中,不能判断此流程的第Ⅱ步反应达到平衡的是②③.
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
(4)如图2表示此流程的第Ⅱ步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是降低温度、增加水蒸汽的量(或减少氢气的量)(写出两种).若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变).

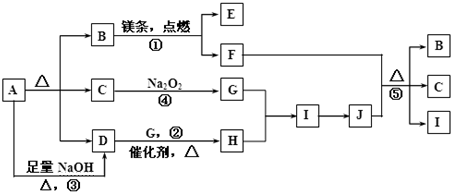
 ;元素C的原子组成符号是2713Al.
;元素C的原子组成符号是2713Al.