题目内容
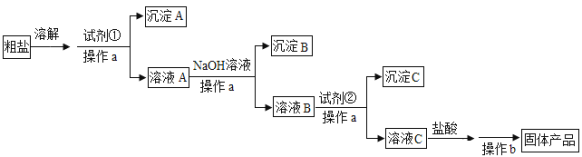
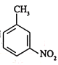
【题目】磷铁(含P、Fe、Cr等)是磷化工生产过程中产生的副产物,一种以磷铁为原料制备![]() 和
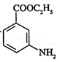
和![]() 的流程如图所示:
的流程如图所示:
已知:水浸后溶液的主要成分为![]() 和
和![]() ;
;![]() 的
的![]() 回答下列问题:
回答下列问题:
(1)“破碎”的目的为________________________________________________________。
(2)“焙烧”时,应将原料加到________坩埚中(填“陶瓷”或“钢制”),原因是_____________(结合化学方程式解释),Cr单质发生的主要反应的化学方程式为________。
(3)进一步提纯粗磷酸钠晶体的方法为________________。
(4)“酸化”时发生反应的离子方程式为________________________________________________。
(5)“沉铬”时,加NaOH调节至pH为________时,铬离子刚好沉淀完全。(已知:![]() ,离子浓度为10-5mol/L时可认为该离子沉淀完全)
,离子浓度为10-5mol/L时可认为该离子沉淀完全)
【答案】增大反应物的接触面积,提高培烧速率,使焙烧更充分 钢制 ![]() ,腐蚀陶瓷坩埚
,腐蚀陶瓷坩埚 ![]() 重结晶
重结晶 ![]() 5.48
5.48
【解析】
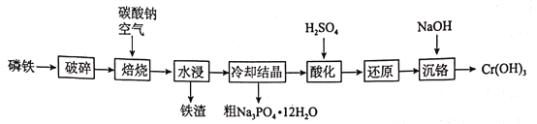
将磷铁(含P、Fe、Cr等)粉碎后和碳酸钠混合并在空气中焙烧,用水溶解过滤除去铁渣,水浸液的主要成分为![]() 和
和![]() ,将水浸液蒸发浓缩并冷却结晶,过滤后即得到Na3PO412H2O的粗产品,滤液用稀硫酸酸化后,继续还原得到Cr3+的溶液,再加入NaOH调节溶液的pH,即可得到Cr(OH)3沉淀,再经过过滤操作即得产品,据此分析解题。
,将水浸液蒸发浓缩并冷却结晶,过滤后即得到Na3PO412H2O的粗产品,滤液用稀硫酸酸化后,继续还原得到Cr3+的溶液,再加入NaOH调节溶液的pH,即可得到Cr(OH)3沉淀,再经过过滤操作即得产品,据此分析解题。
(1)焙烧前先将磷铁粉碎,可增大反应物的接触面积,达到提高培烧速率,使焙烧更充分的目的;
(2)因高温下碳酸钠和SiO2能反应生成硅酸钠和CO2,陶瓷中含有SiO2,则“焙烧”磷铁和碳酸钠混合物时,应将原料加到铁制坩埚中,可防止发生反应:![]() ,避免腐蚀陶瓷坩埚;焙烧时Cr单质和Na2CO3在氧气中发生反应生成Na2CrO4和CO2,发生的主要反应的化学方程式为
,避免腐蚀陶瓷坩埚;焙烧时Cr单质和Na2CO3在氧气中发生反应生成Na2CrO4和CO2,发生的主要反应的化学方程式为![]() ;
;
(3)粗磷酸钠晶体混有![]() ,可结合两者的溶解度随温度变化情况,可通过重结晶提纯得到精制的磷酸钠晶体;
,可结合两者的溶解度随温度变化情况,可通过重结晶提纯得到精制的磷酸钠晶体;
(4)将![]() 溶液“酸化”得到Na2Cr2O7,发生反应的离子方程式为
溶液“酸化”得到Na2Cr2O7,发生反应的离子方程式为![]() ;
;
(5)已知Ksp[Cr(OH)3]=c(Cr3+)×c3(OH-)=2.7×10-31,当c(Cr3+)=10-5mol/L,c(OH-)=![]() mol/L=3×10-9 mol/L,此时溶液的pH=14-9+lg3=5.48。
mol/L=3×10-9 mol/L,此时溶液的pH=14-9+lg3=5.48。