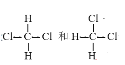题目内容
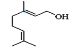
【题目】W、X、Y、Z四种短周期元素的原子序数依次增大,W的某种原子无中子,X、Y可形成原子个数比为![]() 的具有漂白性的物质,工业上常用电解饱和
的具有漂白性的物质,工业上常用电解饱和![]() 溶液来获得Z的单质及其他产品。下列说法正确的是( )
溶液来获得Z的单质及其他产品。下列说法正确的是( )
A.W和X 、Y 、Z均能形成18电子的分子
B.X 、Y 之间形成的化合物可能同时含有离子键和非极性共价健
C.上述四种元素的原子半径大小顺序为![]()
D.W、X 、Z三种元素形成的化合物一定是弱酸
【答案】B
【解析】
W、X、Y、Z四种短周期元素的原子序数依次增大,W的某种原子无中子,则W为H元素;工业上常用电解饱和食盐水获得氢氧化钠、氯气和氢气,则YZ为NaCl,X、Y可形成原子个数比为1:1的具有漂白性的物质为Na2O2,X为Na,Y为O,即:W、X、Y、Z分别为:H、O、Na、Cl,结合原子结构特点及元素性质解答。
依据上述分析可知:W、X、Y、Z分别为:H、O、Na、Cl;
A. 氢与钠形成化合物为NaH,含有电子数为12,故A错误;
B. X 、Y 之间形成的化合物可以为Na2O2,同时含有离子键和非极性共价健,故B正确;
C. 电子层不同的电子层越多,原子半径越大,电子层相同的,原子序数越大,原子半径越小,所以上述四种元素的原子半径大小顺序为:r(Na)>r(Cl)>r(O)>r(H),即:r(Y)>r(Z)>r(X)>r(W),故C错误;
D. W、X、Z三种元素形成的化合物可以为HClO4,高氯酸为强酸,故D错误;
故选B。

【题目】下列实验操作,现象和结论都正确的是
选项 | 操作 | 现象 | 结论 |
A | 用坩埚钳夹一块铝箔在酒精灯上灼烧 | 铝箔熔化并滴落 | 氧化铝的熔点较低 |
B | 向亚硫酸钠溶液中滴加足量盐酸,将产生的气体通入品红溶液 | 品红溶液褪色 | 非金属性: |
C | 将用砂纸除去保护膜的镁片和铝片(大小、形状相同),分别插入同浓度的稀硫酸中 | 镁片表面产生气泡速率大于铝片 | 还原性: |
D | 常温下,将两根大小相同的铁钉分别插入浓硝酸和稀硝酸中 | 浓硝酸中无明显现象,稀硝酸中产生气泡 | 稀硝酸的氧化性比浓硝酸强 |
A.AB.BC.CD.D