题目内容
7.短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数与电子层数相等,则下列说法正确的是( )| A. | 原子半径:丁>丙>乙>甲 | |
| B. | 单质的还原性:丁>丙>甲 | |
| C. | 甲、乙、丙的氧化物均为共价化合物 | |
| D. | 乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
分析 短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,乙位于第VA族,则甲为H,乙为N;甲和丙同主族,丙为Na;丁的最外层电子数和电子层数相等,则丁在第三周期第ⅢA族,即丁为Al,以此来解答.
解答 解:短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,乙位于第VA族,则甲为H,乙为N;甲和丙同主族,丙为Na;丁的最外层电子数和电子层数相等,则丁在第三周期第ⅢA族,即丁为Al.
A.同周期原子半径从左向右减小,电子层越多原子半径越大,则原子半径为丙>丁>乙>甲,故A错误;
B.金属性越强,单质的还原性越强,则单质的还原性丙>丁>甲,故B错误;
C.甲、乙的氧化物为共价化合物,丙的氧化物为离子化合物,故C错误;
D.乙、丙、丁的最高价氧化物对应的水化物分别为硝酸、氢氧化钠、氢氧化铝,硝酸与氢氧化钠发生中和反应,氢氧化铝为两性氢氧化物,能与硝酸、氢氧化钠反应,故D正确,
故选D.
点评 本题考查元素周期律及元素对应的单质化合物的性质,元素的推断是解答本题的关键,注意氨气的水溶液为碱性是解答本题的突破口,难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
17.下列粒子属等电子体的是( )
| A. | SO2和O3 | B. | CH4和NH4+ | C. | NH2-和H2O2 | D. | HCl和H2O |
18.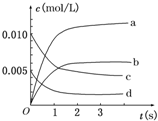 在2L密闭容器内,800℃时反应2SO2(g)+O2(g)?2SO3(g)体系中,n(SO2)随时间的变化如下表:
在2L密闭容器内,800℃时反应2SO2(g)+O2(g)?2SO3(g)体系中,n(SO2)随时间的变化如下表:
(1)用O2表示0~2s内该反应的平均速率v=0.0015mol/(L•s);
(2)图中a、b、c、d四条曲线中表示SO3浓度随时间变化的是b;
(3)恒温恒容条件下,能说明该反应已达到平衡状态的是BC.
A.v(SO3)=2v(O2) B.容器内压强保持不变
C.v逆(SO2)=2v正(O2) D.容器内密度保持不变.
 在2L密闭容器内,800℃时反应2SO2(g)+O2(g)?2SO3(g)体系中,n(SO2)随时间的变化如下表:
在2L密闭容器内,800℃时反应2SO2(g)+O2(g)?2SO3(g)体系中,n(SO2)随时间的变化如下表:| 时间 | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中a、b、c、d四条曲线中表示SO3浓度随时间变化的是b;
(3)恒温恒容条件下,能说明该反应已达到平衡状态的是BC.
A.v(SO3)=2v(O2) B.容器内压强保持不变
C.v逆(SO2)=2v正(O2) D.容器内密度保持不变.
15.如图是某只含有C、H、O、N的有机物简易球棍模型.下列关于该有机物的说法错误的是( )
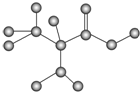

| A. | 该有机物的分子式为C3H7O2N | B. | 该有机物的名称为α氨基丙酸 | ||
| C. | 该有机物能发生加成反应 | D. | 该有机物分子之间能发生聚合反应 |
2.如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )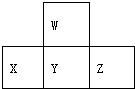

| A. | 元素X的最高价氧化物对应水化物的化学式为H3PO4 | |
| B. | 元素Y有2种氧化物且都能与元素W的氢化物反应生成对应价态的酸 | |
| C. | X、Y、Z各元素最高价和最低价的绝对值之和为8 | |
| D. | 原子半径的大小顺序是Z>Y>X>W |
12.既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中混有的乙烯的方法是( )
| A. | 通入足量溴水中 | B. | 在空气中燃烧 | ||
| C. | 通入饱和食盐水中 | D. | 通入澄清石灰水 |
19.下列说法或表示方法正确的是( )
| A. | 等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 | |
| B. | 由C(石墨)→C(金刚石)△H=+11.9kJ•mol-1可知,金刚石比石墨稳定 | |
| C. | 在25℃,101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3kJ |
16.下列各组微粒具有相同的质子数和电子数的是( )
| A. | OH-、H2O、F- | B. | Na+、NH4+、H3O+ | C. | H3O+、NH4+、NH2- | D. | Cl-、K+、H2S |