题目内容
下列各组离子,在溶液中可以大量共存的是( )
| A、Na+ Ca2+ Cl- CO32- |
| B、K+ NH4+ SO42- NO3- |
| C、Na+ H+ Cl- OH- |
| D、Ba2+ Ca2+ Cl- SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.钙离子与碳酸根离子反应生成难溶物碳酸钙;
B.K+ NH4+ SO42- NO3-离子之间不满足离子反应发生条件;
C.氢离子与氢氧根离子反应生成水;
D.钡离子、钙离子与硫酸根离子反应生成沉淀.
B.K+ NH4+ SO42- NO3-离子之间不满足离子反应发生条件;
C.氢离子与氢氧根离子反应生成水;
D.钡离子、钙离子与硫酸根离子反应生成沉淀.
解答:
解:A.Ca2+、CO32-之间发生反应生成碳酸钙沉淀,在溶液中不能大量共存,故A错误;
B.K+ NH4+ SO42- NO3-之间不发生反应,在溶液中能够大量共存,故B正确;
C.H+、OH-之间能够反应生成水,在溶液中不能大量共存,故C错误;
D.Ba2+、Ca2+与SO42-发生反应,在溶液中不能大量共存,故D错误;
故选B.
B.K+ NH4+ SO42- NO3-之间不发生反应,在溶液中能够大量共存,故B正确;
C.H+、OH-之间能够反应生成水,在溶液中不能大量共存,故C错误;
D.Ba2+、Ca2+与SO42-发生反应,在溶液中不能大量共存,故D错误;
故选B.
点评:本题考查离子共存的正误判断,为高考中的高频题,透明难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等,试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
将1mol冰醋酸加入到一定量的蒸馏水中最终得到1L溶液.下列各项中表征醋酸已达到电离平衡状态的是( )
| A、醋酸的浓度达到1mol?L-1 |
| B、H+的浓度达到0.5mol?L-1 |
| C、醋酸的浓度、醋酸根离子的浓度、H+的浓度均为0.5mol?L-1 |
| D、醋酸分子电离成离子的速率和离子重新结合成分子的速率相等 |
设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L氦气中含有的电子数为2NA |
| B、11g的2H218O分子中含NA个中子 |
| C、1mol NH4+离子所含的质子总数为10NA |
| D、电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g |
离子方程式H++OH-=H2O可表示的化学方程式是( )
| A、盐酸与氢氧化铜的反应 |
| B、硫酸与氢氧化钠的反应 |
| C、硫酸与氢氧化镁的反应 |
| D、盐酸与氨水的反应 |
下列各项表达式正确的是( )
A、S原子的结构示意图: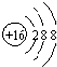 |
| B、过氧化钠的结构式:Na-O-O-Na |
| C、K+离子的核外电子排布式:1s22s22p63s23p6 |
| D、丙烯酸(CH2=CHCOOH)分子中含9个σ键,1个π键 |
在25℃时,用蒸馏水稀释1mol/L氨水至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A、
| ||||
B、
| ||||
C、
| ||||
| D、OH-物质的量 |
下列溶液中的Cl-浓度与50mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A、150mL 2mol/L KCl溶液 |
| B、75mL 1mol/L CaCl2溶液 |
| C、150mL 1mol/L NaCl溶液 |
| D、75mL 1mol/L AlCl3溶液 |
下列物质中,按照只有氧化性、只有还原性,既有氧化性又有还原性的顺序排列的一组是( )
| A、F2、K、HCl |
| B、Cl2、Al、H2 |
| C、NO2、Na、HNO3 |
| D、O2、SO2、H2O |