题目内容
下列各项表达式正确的是( )
A、S原子的结构示意图: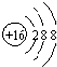 |
| B、过氧化钠的结构式:Na-O-O-Na |
| C、K+离子的核外电子排布式:1s22s22p63s23p6 |
| D、丙烯酸(CH2=CHCOOH)分子中含9个σ键,1个π键 |
考点:原子结构示意图,结构式,原子核外电子排布
专题:化学用语专题
分析:A.S原子的核外有16个电子;
B.过氧化钠为离子化合物,Na与O不能形成共价键;
C.K+离子的核外有18个电子,分三层排布;
D.根据分子中的单键和双键的数目判断.
B.过氧化钠为离子化合物,Na与O不能形成共价键;
C.K+离子的核外有18个电子,分三层排布;
D.根据分子中的单键和双键的数目判断.
解答:
解:A.S原子的核外有16个电子,分三层排布,最外层6个电子,硫原子的结构示意图为: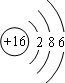 ,故A错误;
,故A错误;
B.过氧化钠为离子化合物,Na与O不能形成共价键,所以过氧化钠不能写结构式,故B错误;
C.K+离子的核外有18个电子,分三层排布,其核外电子排布式:1s22s22p63s23p6,故C正确;
D.丙烯酸(CH2=CHCOOH)分子中含有4个C-H,1个C-C,1个O-H,1个C-O,1个C=C和1个C=O,共9个σ键,2个π键,故D错误;
故选C.
 ,故A错误;
,故A错误;B.过氧化钠为离子化合物,Na与O不能形成共价键,所以过氧化钠不能写结构式,故B错误;
C.K+离子的核外有18个电子,分三层排布,其核外电子排布式:1s22s22p63s23p6,故C正确;
D.丙烯酸(CH2=CHCOOH)分子中含有4个C-H,1个C-C,1个O-H,1个C-O,1个C=C和1个C=O,共9个σ键,2个π键,故D错误;
故选C.
点评:本题考查了电子排布式、原子结构示意图、结构式的判断、共价键等,题目难度不大,注意掌握常见化学用语的概念及表示方法.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
如图所示实验合理的是( )
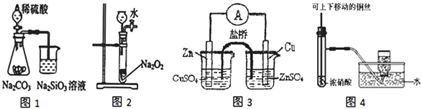

| A、图1证明非金属性强弱:S>C>Si |
| B、图2可制备少量氧气 |
| C、图3构成铜锌原电池,产生持续稳定的电流 |
| D、图4可制备并收集NO2气体 |
下列化学用语表示正确的是( )
A、CO(NH2)2的电子式: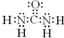 |
| B、NaHCO3的电离方程式:NaHCO3═Na++H++CO32- |
| C、1-丙醇的结构简式:C3H7OH |
| D、含18个中子的氯原子的核素符号:3517Cl |
下列各组物质充分反应后,滴入KSCN溶液一定显红色的是( )
| A、FeO放入稀HCl中 |
| B、FeCl3、CuCl2的混合溶液中加入过量的铁粉 |
| C、Fe(NO3)2固体溶于稀H2SO4中 |
| D、Fe放入HNO3溶液中 |
下列关于实验操作中先后顺序的叙述错误的是( )
| A、实验室制取气体时,先装药品,再检查装置气密性 |
| B、用托盘天平称量药品时,先调节天平平衡,再称量 |
| C、实验室用CO与Fe2O3反应制取铁时,先通CO,再点燃酒精灯 |
| D、稀释浓硫酸时,先在烧杯内倒入水,再缓慢注入浓硫酸,并不断搅拌 |
下列各组离子,在溶液中可以大量共存的是( )
| A、Na+ Ca2+ Cl- CO32- |
| B、K+ NH4+ SO42- NO3- |
| C、Na+ H+ Cl- OH- |
| D、Ba2+ Ca2+ Cl- SO42- |
下列有关化学用语表示正确的是( )
A、N2的电子式: |
| B、质子数为53、中子数为78的碘原子:131I |
| C、HClO的结构简式:H-Cl-O |
D、S2-的结构示意图: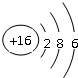 |
对体积不变的气体反应,升高温度时,化学反应速率加快,主要原因是( )
| A、分子运动速率加快,使反应物分子间的碰撞机会增多 |
| B、反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| C、该反应的过程是吸热的 |
| D、该反应的过程是放热的 |