��Ŀ����
����Ŀ������Ӧ�úʹ������Ļ��������������������Ҫ���塣
��1������[CO(NH2)2]��һ�ָ�Ч���ʣ�Ҳ��һ�ֻ���ԭ�ϡ�
��CO(NH2)2(s)+H2O(1)2HN3(g)+CO2(g)��H=+133.6kJ/mol�����ڸ÷�Ӧ������˵����ȷ����____________������ţ���
a.�ӷ�Ӧ��ʼ��ƽ��ʱ�����л�������ƽ����Է����������ֲ���
b.��ƽ����ϵ������ˮ��������ʹ�÷�Ӧ��ƽ�ⳣ������
c.�����¶ȿ�ʹ���ص�ת��������
d.�ﵽƽ�����С�����������ƽ�����淴Ӧ�����ƶ����ﵽƽ��ʱNH3��Ũ�ȴ���ԭƽ��
��������һ�������¿ɽ����������ﻹԭΪ������

��֪��
�ٽ�Ϣ��е���Ϣ����Ӧ2CO(NH2)2(s)+6NO(g)5N2(g)+2CO2(g)+4H2O(1)�Ħ�H=______kJ/mol��
���ܱ��������Ե����ʵ�����NH3��CO2Ϊԭ�ϣ���120�桢����������Ӧ�������أ�CO2(g)+2NH3(g)CO(NH2)2(s)+H2O(g)�����������NH3�����ʵ����ٷֺ�����ʱ��仯��ϵ��ͼ��ʾ��������ƽ��ת����Ϊ____________
��2��NO2����Ⱦ����������Na2CO3��Һ����NO2������CO2����֪9.2gNO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol��ǡ�÷�Ӧ��ʹ��Һ�е�CԪ��ȫ����CO2��ʽ�ݳ���������Һ�������ԣ�����Һ������Ũ�ȴ�С��ϵ��c(Na+)��_________________________��
��3������ȼ�ϵ��Ϊ��Դ��ͨ�����ӽ���Ĥ��ⷨ���Ƶ��Һ��OH��Ũ�����Ʊ�����Cu2O��װ����ͼ��ʾ��

����װ����������ӦʽΪ_________________________���õ����е����ӽ���ĤΪ______________������������������ӽ���Ĥ��
���𰸡�a -1804.7kJ/mol 75% c(NO3-)��c(NO2-)��c(OH-)��c(H+) 2Cu-2e-+2OH===Cu2O+H2O ��
��������
��1��
��a. �÷�Ӧ��ֻ�������������壬���ɵİ����Ͷ�����̼���������ʵ�����ֵ���䣻
b. ��ѧƽ�ⳣ��ֻ���¶�Ӱ�죻
c. ����ƽ���������ƶ���
�ڽ��ͼ����Ϣ�����ݸ�˹���ɰ�Ҫ����㷴Ӧ�ȣ�
�����ݰ���������������ƽ������ʽ��ʽ����ƽ��ת���ʣ�
��2��9.2g NO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol����ÿ2mol NO2��Na2CO3��Һ��Ӧʱת�Ƶ���1mol�������ɵ����ᣬ���ݻ��ϼ۵ı仯�ж�������Դ���д��Ӧ�����ӷ���ʽ��
��3�����ݵ��ԭ������������������Ӧ��ͭʧ����ת��Ϊ������ͭ���ݴ˷�������
(1)
a. ���������ֻ�а�����������̼���������ʵ���֮��Ϊ��ֵ2:1��ƽ����Է����������䣬 a����ȷ��
b.ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣬����ˮ��������Ӱ��ƽ�ⳣ����b�����
c.����ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ������ص�ת���ʼ�С��c�����
�ʴ�Ϊ��a��
��������һ�������¿ɽ����������ﻹԭΪ��������Ӧ����ʽΪ��2CO(NH2)2(s)+6NO(g)=5N2(g)+2CO2(g)+4H2O(l)��
��֪����CO(NH2)2(s)+H2O(l)2NH3(g)+CO2(g) ��H=+133.6kJ/mol��
��ͼ�ɵ��Ȼ�ѧ����ʽ����4NH3(g)+6NO(g)=5N2(g)+6H2O(l) ��H=2071.9kJ/mol��
���ݸ�˹����,����2+�ڿɵã�2CO(NH2)2(s)+6NO(g)=5N2(g)+2CO2(g)+4H2O(l) ��H=1804.7 kJ/mol��
�ʴ�Ϊ�� 1804.7 kJ/mol��
����NH3��CO2����ʼ���ʵ���Ϊ1 mol��ƽ��ʱ����ת����Ϊx����
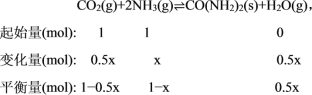 ���������������=
���������������=![]() �����x = 75%��
�����x = 75%��
�ʴ�Ϊ��75%��
(2)9.2 gNO2�����ʵ���![]() =0.2mol��Na2CO3��Һ��ȫ��Ӧ����CO2ʱת�Ƶ���0.1mol����Ӧ��ֻ��NԪ�ػ��ϼ۱仯����N�Ļ��ϼ۷ֱ���+4�۱仯Ϊ+5�ۺ�+3�ۣ���Ӧ�����ӷ���ʽΪ��2NO2+CO32=NO3+NO2+CO2���ڼ�����Һ��Ӧ����NaNO3��NaNO2,����Ũ����ȣ�NO2ˮ����Һ�ʼ��ԣ�������Һ�е�����Ũ�ȴ�С��ϵΪc(Na+)>c(NO3)>c(NO2)>c(OH)>c(H+)��
=0.2mol��Na2CO3��Һ��ȫ��Ӧ����CO2ʱת�Ƶ���0.1mol����Ӧ��ֻ��NԪ�ػ��ϼ۱仯����N�Ļ��ϼ۷ֱ���+4�۱仯Ϊ+5�ۺ�+3�ۣ���Ӧ�����ӷ���ʽΪ��2NO2+CO32=NO3+NO2+CO2���ڼ�����Һ��Ӧ����NaNO3��NaNO2,����Ũ����ȣ�NO2ˮ����Һ�ʼ��ԣ�������Һ�е�����Ũ�ȴ�С��ϵΪc(Na+)>c(NO3)>c(NO2)>c(OH)>c(H+)��
�ʴ�Ϊ��c(NO3)>c(NO2)>c(OH)>c(H+)��
��3�������ܷ�Ӧ����������ӦΪ2Cu2e+2OH=Cu2O+H2O���������ӽ���ĤӦ���������ӽ���Ĥ��
�ʴ�Ϊ��2Cu2e+2OH=Cu2O+H2O������

 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�