题目内容
1.乙酸乙酯和丙酸的混合物中氧元素质量分数为30%,则氢元素的质量分数为( )| A. | 40% | B. | 30% | C. | 10% | D. | 20% |
分析 乙酸乙酯的分子式为C4H8O2,丙醛的分子式为C3H6O,两种物质中C、H原子的数目之比为1:2,故混合物中C、H元素质量之比为12:2=6:1,则根据氧元素的质量分数可计算化合物中碳、氢元素的总质量分数,进而计算该混合物中氢元素的质量分数.
解答 解:混合物中氧元素的质量分数为30%,则C、H元素总质量分数为1-30%=70%,乙酸乙酯的分子式为C4H8O2,丙醛的分子式为C3H6O,两种物质中C、H原子的数目之比为1:2,故混合物中C、H元素质量之比为12:2=6:1,故氢元素质量分数为70%×$\frac{1}{1+6}$=10%,故选C.
点评 本题考查元素质量分数的计算,难度不大,关键是根据分子式确定混合物中C、H元素的质量关系.

练习册系列答案
相关题目
11.在某些高档点心的包装盒内有个小纸袋,将小纸袋打开,可看到灰黑色粉末,其中有些已变成棕褐色.将灰黑色粉末溶于盐酸,取上层清液,滴入几滴氯水,再滴入KSCN溶液,马上出现血红色.以下结论不正确的是( )
| A. | 该灰黑色粉末用作抗氧化剂 | B. | 小袋中的原装粉末是Fe2O3 | ||
| C. | 小袋中可能装有活性铁粉 | D. | 该灰黑色粉末不可食用 |
16.下列叙述不正确的是( )
| A. | 金刚石晶胞(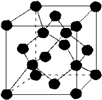 )中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8 )中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8 | |
| B. | 二氧化硅晶体中最小环上的氧原子数、氯化铯晶体中氯离子的配位数均为6 | |
| C. | 锌晶胞 中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12 中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12 | |
| D. | 33g CH≡C-CH=CH-CH3中所含的π键数、12g石墨中所含的碳碳键数均为1.5mol. |
6.已知反应:X+Y=M+N 为放热反应,对该反应的下列说法中正确的是( )
| A. | X 的能量一定高于 M | |
| B. | X 和 Y 的总能量一定高于 M 和 N 的总能量 | |
| C. | Y 的能量一定高于 N | |
| D. | 因为该反应是放热反应,故不必加热反应就一定能发生 |
10.某有机物的结构简式为: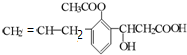 ,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦缩聚 ⑧中和 则( )
,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦缩聚 ⑧中和 则( )
 ,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦缩聚 ⑧中和 则( )
,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦缩聚 ⑧中和 则( )| A. | 除①⑥外均能 | B. | 除①⑦外均能 | C. | 除⑥⑦外均能 | D. | 以上反应均能 |