��Ŀ����
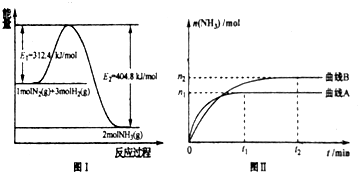
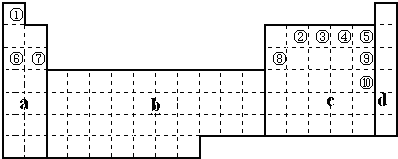
���ֶ�����Ԫ�������ڱ��е����λ��������ʾ������ZԪ������������������Ӳ�����2������ش��������⣺
��1��Ԫ��Zλ�����ڱ��е�λ�� ��
��2��ʵ������ȡXԪ�ص��⻯��Ļ�ѧ����ʽΪ ��
��3��W��Z������������Ӧ�ĺ���������� �� ���û�ѧʽ��ʾ����
��4����W�ĵ���ͨ�뺬�����ʵ���FeBr2����Һ�У�������Ӧ�����ӷ���ʽΪ ��
��5��Z��X�γɵ�һ�ֻ�������Է���������170��190֮�䣬��Z����������ԼΪ70%���û�����Ļ�ѧʽΪ ��
| X | Y | |
| Z | W |
��2��ʵ������ȡXԪ�ص��⻯��Ļ�ѧ����ʽΪ
��3��W��Z������������Ӧ�ĺ����������
��4����W�ĵ���ͨ�뺬�����ʵ���FeBr2����Һ�У�������Ӧ�����ӷ���ʽΪ
��5��Z��X�γɵ�һ�ֻ�������Է���������170��190֮�䣬��Z����������ԼΪ70%���û�����Ļ�ѧʽΪ
���㣺Ԫ�������ɺ�Ԫ�����ڱ����ۺ�Ӧ��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
�������ɶ�����Ԫ�������ڱ��е����λ�ã���֪X��Y���ڵڶ����ڣ�Z��W���ڵ������ڣ�ZԪ������������������Ӳ�����2��������������Ϊ6����ZΪSԪ�أ�����֪WΪCl��YΪO��XΪN���ݴ˽��
���
�⣺�ɶ�����Ԫ�������ڱ��е����λ�ã���֪X��Y���ڵڶ����ڣ�Z��W���ڵ������ڣ�ZԪ������������������Ӳ�����2��������������Ϊ6����ZΪSԪ�أ�����֪WΪCl��YΪO��XΪN��
��1��Ԫ��ZΪS�������ڱ��е�λ���ǣ��������ڵڢ�A�壬�ʴ�Ϊ���������ڵڢ�A�壻
��2��XԪ�ص��⻯��Ϊ������ʵ������ȡ�����Ļ�ѧ����ʽΪ��2NH4Cl+Ca��OH��2
CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2
CaCl2+2NH3��+2H2O��
��3���ǽ�����Cl��S��������������Ӧ�ĺ���������ԣ�HClO4��H2SO4���ʴ�Ϊ��HClO4��H2SO4��
��4���������ĵ���ͨ�뺬�����ʵ���FeBr2����Һ�У������������������ӣ������������ӣ�����������FeBr2��Ϊ1mol�����ݵ���ת���غ㣬������1mol����������Ҫ����Ϊ
=0.5mol��ʣ��0.5mol���������ݵ���ת���غ㣬0.5mol������������1mol�����ӣ��ʷ�Ӧ�����ӷ���ʽΪ��2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-���ʴ�Ϊ��2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-��
��5��S��N�γɵ�һ�ֻ�������Է���������170��190֮�䣬��S����������ԼΪ70%����NԪ����������Ϊ30%���������S��Nԭ����Ŀ֮��=
��
��1��1�������ʽΪ��SN��n����170��46n��190������ȷ��3.7��n��4.13����n=4�������ʽΪ��S4N4���ʴ�Ϊ��S4N4��
��1��Ԫ��ZΪS�������ڱ��е�λ���ǣ��������ڵڢ�A�壬�ʴ�Ϊ���������ڵڢ�A�壻
��2��XԪ�ص��⻯��Ϊ������ʵ������ȡ�����Ļ�ѧ����ʽΪ��2NH4Cl+Ca��OH��2
| ||
�ʴ�Ϊ��2NH4Cl+Ca��OH��2
| ||
��3���ǽ�����Cl��S��������������Ӧ�ĺ���������ԣ�HClO4��H2SO4���ʴ�Ϊ��HClO4��H2SO4��
��4���������ĵ���ͨ�뺬�����ʵ���FeBr2����Һ�У������������������ӣ������������ӣ�����������FeBr2��Ϊ1mol�����ݵ���ת���غ㣬������1mol����������Ҫ����Ϊ
| 1mol |
| 2 |
��5��S��N�γɵ�һ�ֻ�������Է���������170��190֮�䣬��S����������ԼΪ70%����NԪ����������Ϊ30%���������S��Nԭ����Ŀ֮��=
| 70% |
| 32 |
| 30% |
| 14 |
���������⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ�����4�������ӷ���ʽ��д��ע�����ӷ�Ӧ���Ⱥ�˳����������ϵ���Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
�������������л�����ǣ�������
| A���軯�� KCN |
| B������� NH4CNO |
| C������Ȳ ��C2H2��n |
| D��̼���� SiC |

 ͼ��X��Y��Z��W�ǵؿǺ���ǰ��λ������˳��Ԫ����ɵĵ��ʣ�����Ϊ�����A�д��ԣ�����֮���������ת����ϵ�����ֲ�������ȥ����
ͼ��X��Y��Z��W�ǵؿǺ���ǰ��λ������˳��Ԫ����ɵĵ��ʣ�����Ϊ�����A�д��ԣ�����֮���������ת����ϵ�����ֲ�������ȥ����