题目内容
【题目】已知A、B、C为中学化学中常见的单质,在室温下A为固体,B和C为气体,向D溶液中加入KSCN溶液后,溶液显红色。在适宜的条件下可发生如下关系的化学反应。
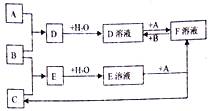
回答以下问题:
(1)写出B的化学式:____________
(2)写出E溶液和+A→F溶液+C的离子反应方程式:___________________。D溶液和+A→F溶液的离子反应方程式:_______________________________。若向F溶液中加入NaOH溶液,观察到的现象为:________________________。
(3)写出除去D溶液中F杂质的离子反应方程式:__________________________。
【答案】Cl2 Fe+2H+=Fe2++H2↑ 2Fe3++Fe=3Fe2+ 溶液中生成白色沉淀,迅速变灰绿色,最终变红褐色 2Fe2++Cl2=2Fe3++2Cl-
【解析】
A. B. C为中学化学中常见的单质,在室温下A为固体,B和C为气体,A与B反应生成D,向D溶液中加入KSCN溶液后,溶液显红色,说明D溶液中含有Fe3+,由D溶液与F溶液的相互转化关系可知,A为Fe,B为Cl2,D为FeCl3,F为FeCl2,B与C反应生成E,Fe与E溶液反应得到氯化亚铁与C,则C为H2,E为HCl。
(1).根据上述分析可知,B为Cl2,故答案为:Cl2;
(2). E为HCl,A为Fe,则E溶液和A反应的离子方程式为:Fe+2H+=Fe2++H2↑;D为FeCl3,与Fe反应的离子方程式为:2Fe3++Fe=3Fe2+;F为FeCl2,向F溶液中加入NaOH溶液,FeCl2与NaOH反应生成Fe(OH)2白色沉淀,Fe(OH)2迅速被空气中的氧气氧化生成Fe(OH)3,所以观察到的实验现象是:溶液中生成白色沉淀,迅速变灰绿色,最终变红褐色,故答案为:Fe+2H+=Fe2++H2↑;2Fe3++Fe=3Fe2+;溶液中生成白色沉淀,迅速变灰绿色,最终变红褐色;
(3). D为FeCl3,F为FeCl2,除去FeCl3溶液中FeCl2杂质,可以向溶液中通入足量的氯气,将Fe2+氧化为Fe3+,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-。

【题目】铜阳极泥是有色金属冶炼过程中重要的“二次资源”。其合理处理对于实现资源的综合利用具有重要意义。一种从铜阳极泥中分离提取多种金属元素的工艺流程如下:
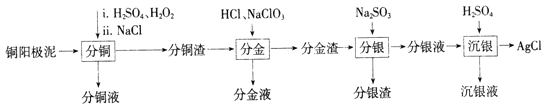
已知:分金液的主要成分为[AuCl4]-;分金渣的主要成分为AgCl和PbSO4;分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-![]() Ag++2SO32-。
Ag++2SO32-。
(1)①“分铜”时,单质铜发生反应的化学方程式为________;反应过程中需控制适当温度,温度不宜过高或过低的原因为_______。
②已知“分铜”时 各元素的浸出率如下表所示。
Cu | Au | Ag | |
浸出率/% | 85.7 | 0 | 4.5 |
“分铜”时加入足量的NaCl的主要作用为__________
(2)“分金”时,单质金发生反应的离子方程式为___________。
(3)“沉银”时,需加入硫酸调节溶液的pH=4。已知: ![]() ,其中X表示SO32-、HSO3-或H2SO3,δ(x)与PH的关系如图所示。
,其中X表示SO32-、HSO3-或H2SO3,δ(x)与PH的关系如图所示。
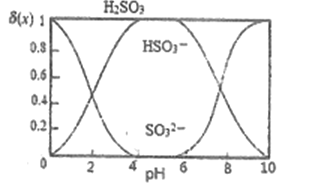
①分析能够析出AgCl的原因为_________
②调节溶液的PH不能过低,理由为__________
(4)“沉银液”加碱调至pH=8.0,Na2SO3可再生并循环利用,其再生原理为____(用离子方程式表示)。
(5)已知离子浓度≤10-5mol/L时,认为该离子沉淀完全;Ksp[Pb(OH)2]=2.5×10-16.
Ksp[Sb(OH)3])=10-41. 浸取“分银渣”可得到含0.025mol/L Pb2+的溶液( 含少量Sb3+杂质)。欲获得较纯净的Pb2+溶液,调节PH的范围为________。 (忽略溶液体积变化)