题目内容
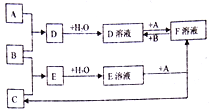
【题目】(1)某元素M,其离子M2+,M2+原子核核内有20个中子,核外有18个电子,则M的质子数是__________,质量数是_________
(2)根据下列叙述,写出微粒符号和结构示意图。
a.原子核外有2个电子层,核外有10个电子的原子________、______________;
b.质量数为24,质子数等于中子数的原子_________、__________________;
c.最外层电子数是次外层电子数的4倍的二价阴离子_________、_________________。
(3)结构示意图为 的阳离子,其电子式符号可能为________、________、________。
的阳离子,其电子式符号可能为________、________、________。
【答案】 20 40 Ne ![]() Mg
Mg ![]() O2-
O2- ![]() Na+ Mg2+ Al3+
Na+ Mg2+ Al3+
【解析】试题分析:(1)阳离子的核外电子数=质子数—电荷数;质量数=质子数+中子数;(2)a.核外有10个电子的原子是Ne;b. 质量数为24,而质量数=质子数+中子数,质子数=中子数,所以质子数=12,该原子是Mg;c.最外层电子数是次外层电子数的4倍的二价阴离子是O2-;(3)结构示意图为 的阳离子,可能是钠离子、镁离子、铝离子;
的阳离子,可能是钠离子、镁离子、铝离子;
解析:阳离子的核外电子数=质子数—电荷数,M2+核外有18个电子,所以M的质子数是20;质量数=质子数+中子数,M2+原子核核内有20个中子,所以质量数是40;(2)a.核外有10个电子的原子是Ne,原子结构示意图为![]() ;b. 质量数为24,而质量数=质子数+中子数,质子数=中子数,所以质子数=12,该原子是Mg,原子结构示意图为
;b. 质量数为24,而质量数=质子数+中子数,质子数=中子数,所以质子数=12,该原子是Mg,原子结构示意图为![]() ;c.最外层电子数是次外层电子数的4倍的二价阴离子是O2-,结构示意图为
;c.最外层电子数是次外层电子数的4倍的二价阴离子是O2-,结构示意图为![]() ;(3)结构示意图为
;(3)结构示意图为 的阳离子,可能是钠离子、镁离子、铝离子,电子式符号为Na+ 、 Mg2+ 、 Al3+;
的阳离子,可能是钠离子、镁离子、铝离子,电子式符号为Na+ 、 Mg2+ 、 Al3+;

【题目】TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

资料:TiCl4及所含杂质氯化物的性质
化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
沸点/℃ | 58 | 136 | 181(升华) | 316 | 1412 |
熔点/℃ | 69 | 25 | 193 | 304 | 714 |
在TiCl4中的溶解性 | 互溶 | —— | 微溶 | 难溶 | |
(1)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) 2C(s)+O2(g)=2CO(g)
① 沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的化学方程式:________________
② 氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是_____________________。
③ 氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有_____________
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4。示意图如下:
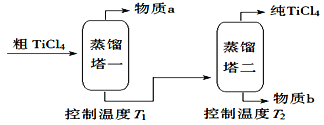
物质a是_________,T2应控制在_________