题目内容
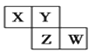
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是( )
A. 元素Y和元素Z的最高正化合价相同
B. 单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z)
C. 元素Y和元素Z的氢化物中均只存在极性共价键
D. 元素W的最高价氧化物对应水化物的酸性最强
【答案】D
【解析】
Y原子的最外层电子数是其电子层数的3倍,Y是O元素,根据X、Y、Z、W在元素周期表中的相对位置可知,X是N元素、Z是S元素、W是Cl元素。
A. O元素的最高正价不是+6,S元素的最高正化合价是+6,故A错误;
B. Cl-、S2-有3个电子层,O2-有2个电子层,单核阴离子半径的大小顺序为:r(S2-)>r(Cl-)>r(O2-),故B错误;
C. H2O2中存在极性共价键O-H和非极性共价键O-O,故C错误;
D. 4种元素中Cl的非金属性最强,最高价氧化物对应水化物中HClO4的酸性最强,故D正确;

练习册系列答案
相关题目