题目内容
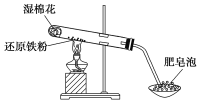
【题目】某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,写出反应的化学方程式并用双线桥法表示出反应中电子转移的方向和数目_____________________;若在标准状况下收集到22.4 L氯气,则被氧化的HCl的物质的量是______。
(2)漂白粉将在U形管中产生,其化学方程式是______________。
(3)C装置的作用是_______________________________________。
(4)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是______________________________________________________________。
②试判断另一个副反应__________________________________(用化学方程式表示)。为避免此副反应的发生,可将装置做何改进________________________________。
【答案】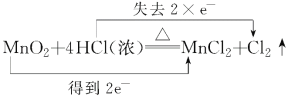 +2H2O2 mol2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O吸收未反应完的氯气,防止污染空气冷却B装置(将B装置放在冷水中)2HCl+Ca(OH)2===CaCl2+2H2O 在A与B之间连接一个装有饱和氯化钠溶液的洗气瓶
+2H2O2 mol2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O吸收未反应完的氯气,防止污染空气冷却B装置(将B装置放在冷水中)2HCl+Ca(OH)2===CaCl2+2H2O 在A与B之间连接一个装有饱和氯化钠溶液的洗气瓶
【解析】
(1)二氧化锰与浓盐酸发生反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,Mn元素化合价由+4价降低到+2价,所以二氧化锰为氧化剂,Cl元素化合价由-1价升高,HCl为还原剂,因此该反应的电子转移方向和数目可表示为
MnCl2+Cl2↑+2H2O,Mn元素化合价由+4价降低到+2价,所以二氧化锰为氧化剂,Cl元素化合价由-1价升高,HCl为还原剂,因此该反应的电子转移方向和数目可表示为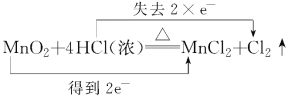 +2H2O;若在标准状况下收集到22.4 L氯气即1mol氯气,根据氯原子守恒可知被氧化的HCl的物质的量是2mol;
+2H2O;若在标准状况下收集到22.4 L氯气即1mol氯气,根据氯原子守恒可知被氧化的HCl的物质的量是2mol;
(2)漂白粉将在U形管中产生,其化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。
(3)氯气有毒需要尾气处理,则C装置的作用是吸收未反应完的氯气,防止污染空气。
(4)①由题意可知,温度较高时容易发生副反应,所以避免此副反应的发生,应该降低体系的温度,因此可以冷却B装置(将B装置放在冷水中);
②由于生成的氯气中含有挥发出的氯化氢,氯化氢能与氢氧化钙反应,则另一个副反应为2HCl+Ca(OH)2=CaCl2+2H2O。为避免此副反应的发生,需要除去氯化氢,则可在A与B之间连接一个装有饱和氯化钠溶液的洗气瓶。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案