题目内容
【题目】海水中有丰富的资源,多种多样的海洋动物和植物,海底有丰富的矿藏、石油、天然气等,此外,海水中还含有大量的电解质,它们电离产生Cl-、Br-、I-、SO42-、Na+、Mg2+、Ca2+等,都是重要资源.开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
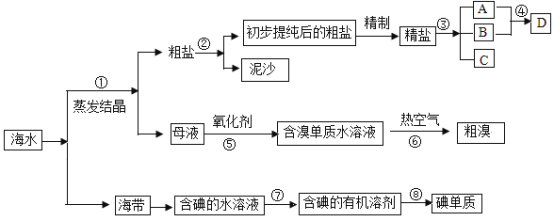
请根据以上信息回答下列问题:
(1)写出步骤②、⑧分离提纯的方法:
②_______⑧_______。
(2)步骤⑦分离提纯过程中需要选用的玻璃仪器除烧杯外,还需要的仪器是_____。
(3)D具有杀菌消毒的作用,请写出反应④的化学方程式_________________。
(4)初步提纯后的粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
①盐酸 ②氯化钡溶液 ③氢氧化钠溶液 ④碳酸钠溶液,
下列试剂添加顺序合理的是_________。
A.②③④① B.③④②① C.④③②① D.③②④①
(5)若用来提取Br2,反应⑤所用的氧化剂的来源较合理的是___________。
A.从外地购买 B.在当地新建生产厂 C.从本厂生产烧碱处循环
(6)流程⑥将溴单质从水溶液中分离出来是基于溴单质具有_______性,该方法对比有机溶剂萃取法的优点是________________________。
【答案】过滤 蒸馏 分液漏斗 Cl2+2NaOH=NaCl+NaClO+H2O AD C 挥发 经济,环保,方便
【解析】
(1)步骤②为过滤,⑧为从有机溶剂中提取碘单质,需要蒸馏,答案为:过滤,蒸馏;
(2)步骤⑦分离提纯方法为萃取,主要玻璃仪器为分液漏斗、烧杯,答案为:分液漏斗;
(3)反应④是氯气和氢氧化钠反应生成次氯酸钠、氯化钠和水,方程式Cl2+2NaOH=NaCl+NaClO+H2O;
(4)镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,但是加入的碳酸钠要放在加入氯化钡之后,这样碳酸钠会同时除去过量的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以添加试剂的顺序为②③④①或③②④①,答案为:AD;
(5)若要提取Br2,反应⑤所用的氧化剂为氯气,本厂电解氯化钠溶液生产烧碱,产物中有氯气,答案为:C;
(6)溴单质具有挥发性,所以流程⑥将溴单质从水溶液中分离出来是基于溴单质具有挥发性;该方法对比有机溶剂萃取法的优点是经济,环保,方便