题目内容
9.下列说法正确的是( )| A. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 | |
| B. | 可逆反应达到平衡后,正、逆反应速率均为0 | |
| C. | 2 mol SO2 与1 mol O2混合一定能生成2 mol SO3 | |
| D. | 使用催化剂不一定能加大反应速率 |
分析 A.氯化氢中只存在H-Cl之间的共价键;
B.可逆反应达到平衡状态时,正逆反应速率相等但不是0;
C.SO2、O2反应生成SO3的反应为可逆反应,反应物不能完全转化为生成物;
D.催化剂可能增大反应速率也可能降低反应速率.
解答 解:A.氯化氢中只存在H-Cl之间的共价键,所以氯化氢是共价化合物,故A错误;
B.可逆反应达到平衡状态时,正逆反应速率相等但不是0,故B错误;
C.SO2、O2反应生成SO3的反应为可逆反应,反应物不能完全转化为生成物,所以2molSO2与1molO2混合一定不能生成2 mol SO3,故C错误;
D.催化剂可能增大反应速率也可能降低反应速率,如果催化剂中毒,则降低反应速率,故D正确;
故选D.
点评 本题考查离子化合物和共价化合物判断、可逆反应等知识点,为高频考点,要根据物质中存在的化学键判断化合物类型,易错选项是D,注意催化剂是改变反应速率而不是一定增大反应速率,为易错点.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案
相关题目
2.下列各操作中,适宜用来制备氢氧化铝的是( )
| A. | 将氧化铝放入水中共热 | |
| B. | 将金属钠投入氯化铝溶液中 | |
| C. | 将足量氨水滴入氯化铝溶液中 | |
| D. | 将足量氢氧化钠溶液滴入氯化铝溶液中 |
20.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1mol/L的NaOH溶液中Na+的物质的量为1mol | |
| B. | 常温常压下,32gO2与O3的混合气体中含有的原子总数为2NA | |
| C. | 0.1mol氯气与足量的铁发生反应,转移的电子为0.3NA | |
| D. | 25℃时,l L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA |
19.将质量分数为a%,物质的量浓度为c1 mol•L-1的稀H2SO4蒸发掉一定量的水,使之质量分数变为2a%,此时该H2SO4的物质的量浓度为c2 mol•L-1,则c1和c2的数值关系是( )
| A. | c2=2c1 | B. | c2>2c1 | C. | c2<2c1 | D. | 无法确定 |

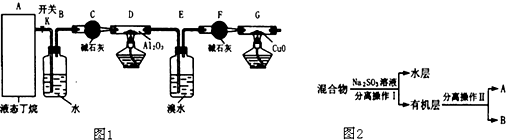

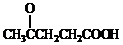 )合成聚芳酯E的路线:
)合成聚芳酯E的路线: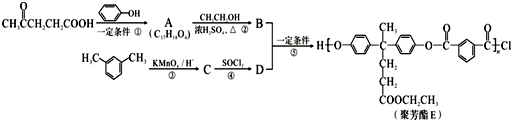
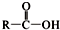 +SOCl2→
+SOCl2→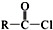 +SO2+HCl
+SO2+HCl +R′OH→
+R′OH→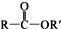 +HCl (R、R′表示烃基)
+HCl (R、R′表示烃基)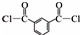 .
.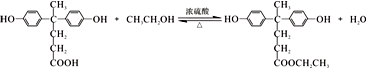 .
. 结构
结构 .
.