题目内容
18.金属钠很容易和空气中氧气、水反应,通常保存在煤油中.分析 空气的主要成分为氮气和氧气,还含有少量的二氧化碳和水蒸气,据此分析能和钠反应的物质;钠由于性质很活泼,故必须隔绝空气和水保存,据此分析.
解答 解:空气的主要成分为氮气和氧气,还含有少量的二氧化碳和水蒸气,钠能和空气中的O2反应生成Na2O,能和H2O反应生成NaOH和H2;
钠由于性质很活泼,能和氧气和水反应,故必须隔绝空气和水保存,应保存在煤油中.
故答案为:氧气,水,煤油.
点评 本题考查了钠的性质和保存,根据钠是一种非常活泼的金属来分析,难度不大.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
9.下列说法正确的是( )
| A. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 | |
| B. | 可逆反应达到平衡后,正、逆反应速率均为0 | |
| C. | 2 mol SO2 与1 mol O2混合一定能生成2 mol SO3 | |
| D. | 使用催化剂不一定能加大反应速率 |
6.将0.15mol的MnO2与过量的12mol/L的浓盐酸反应,与50mL12mol/L的浓盐酸与过量MnO2反应,两者产生的氯气相比(其它反应条件相同)( )
| A. | 一样多 | B. | 后者较前者多 | C. | 前者较后者多 | D. | 无法比较 |
13.下列物质间的转化涉及的反应类型和反应条件都正确的是( )
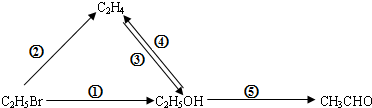

| 选项 | 反应 | 类型 | 反应条件 |
| A | ① | 取代反应 | 氢氧化钠的乙醇溶液、加热 |
| B | ② | 消去反应 | 浓硫酸、加热至170℃ |
| C | ③ | 加成反应 | 催化剂、加热 |
| D | ⑤ | 取代反应 | Cu或Ag作催化剂、加热 |
| A. | A | B. | B | C. | C | D. | D |
3.下列物质中属于有机物的是( )
①酒精;②食盐;③石墨;④甲烷;⑤红糖;⑥水;⑦一氧化碳;⑧石灰石;⑨食用油;⑩醋酸.
①酒精;②食盐;③石墨;④甲烷;⑤红糖;⑥水;⑦一氧化碳;⑧石灰石;⑨食用油;⑩醋酸.
| A. | ①②④⑤⑨ | B. | ①④⑤⑨⑩ | C. | ①③④⑤⑦⑧⑨⑩ | D. | ①④⑤⑥⑩ |
10.下列有关有机物的说法正确的是( )
| A. | 石油的分馏和煤的干馏都属于物理变化 | |
| B. | 苯、四氯化碳和乙醇可用水加以鉴别 | |
| C. | 蔗糖和淀粉在稀硫酸的催化作用下最终水解产物相同 | |
| D. | 乙烯和苯分子中都含有碳碳双键,都能与溴水发生加成反应 |
7. 某同学为探究元素和化合物性质的递变规律,设计了如下系列实验.
某同学为探究元素和化合物性质的递变规律,设计了如下系列实验.
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:钾与盐酸反应最剧烈;铝与盐酸反应的速率最慢铝与盐酸反应产生的气体最多.
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为S2-+Cl2═S↓+2Cl-.
(3)利用如图装置可验证出三种物质性质的递变规律
①仪器B的名称为锥形瓶,干燥管D的作用为防止倒吸.
②若要证明氧化性:KMnO4>Cl2>I2,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液变蓝的现象,即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用NaOH溶液吸收尾气.
③此装置还能验证哪些物质的性质的递变性,请在下表格中填写一组物质并得出实验结论.
 某同学为探究元素和化合物性质的递变规律,设计了如下系列实验.
某同学为探究元素和化合物性质的递变规律,设计了如下系列实验.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:钾与盐酸反应最剧烈;铝与盐酸反应的速率最慢铝与盐酸反应产生的气体最多.
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为S2-+Cl2═S↓+2Cl-.
(3)利用如图装置可验证出三种物质性质的递变规律
①仪器B的名称为锥形瓶,干燥管D的作用为防止倒吸.
②若要证明氧化性:KMnO4>Cl2>I2,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液变蓝的现象,即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用NaOH溶液吸收尾气.
③此装置还能验证哪些物质的性质的递变性,请在下表格中填写一组物质并得出实验结论.
| A中加入物质 | B中加入物质 | C中加入物质 | 实验结论 |
| 稀硫酸或盐酸 | 碳酸钠(或碳酸盐) | 硅酸钠溶液 | 酸性:盐酸>碳酸>硅酸 |
| 氢氧化钠溶液(强碱溶液) | 氯化铵(或铵盐) | 氯化铜溶液(难溶碱的可溶性盐溶液) | 碱性:氢氧化钠>一水合氨>氢氧化铜 |
8.因与人体血液中血红蛋白作用而引起中毒的气体是( )
| A. | NO2 | B. | CO | C. | NH3 | D. | Cl2 |