题目内容
12.下列物质属于共价化合物的是( )| A. | H2O | B. | I2 | C. | NH4Cl | D. | CaCl2 |
分析 非金属元素之间易形成共价键,只含共价键的化合物属于共价化合物,共价化合物中一定不含离子键,据此分析解答.
解答 解:A.水分子中H-O原子之间存在共价键,属于共价化合物,故A正确;
B.碘分子中I-I原子之间只存在共价键,但属于单质,故B错误;
C.氯化铵中铵根离子和氯离子之间存在离子键、铵根离子中N-H原子之间存在共价键,属于离子化合物,故C错误;
D.氯化钙中钙离子和氯离子之间只存在离子键,属于离子化合物,故D错误;
故选A.
点评 本题考查离子键和共价键、单质和化合物的判断,侧重考查基本概念,根据物质构成微粒及基本概念解答即可,注意氯化钙中不含共价键,为易错点.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
2.根据元素周期律,由列事实进行归纳推测,推测不合理的是事实( )
| 事实 | 推测 | |
| A | 12Mg与水反应缓慢,20Ca与水反应较快 | 56Ba(IIA族)与水反应更快 |
| B | Si是半导体材料,同族Ge也是半导体材料 | Ⅳ族的元素都是半导体材料, |
| C | HCl在1500℃时分解,HI在230℃时分解 | HBr的分解温度介于二者之间 |
| D | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
| A. | A | B. | B | C. | C | D. | D |
3.用下列实验装置进行相应实验,能达到实验目的是(夹持装置未画出)( )
| A. | 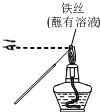 用装置甲检验溶液中是否有K+ | B. | 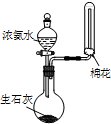 用装置乙制取并收集少量NH3 | ||
| C. | 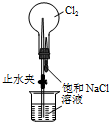 用装置丙进行喷泉实验 | D. |  用装置丁加热熔融NaOH固体 |
7.下列反应所得溶液中只含有一种溶质的是( )
| A. | 稀硝酸中加入过量铜片 | B. | Ca(OH)2溶液中通入Cl2 | ||
| C. | FeCl3溶液中加入过量铜片 | D. | AlCl3溶液中通入过量NaOH溶液 |
17.臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)?N2O5(g)+O2(g).有关说法正确的是( )
| A. | 增大压强可提高反应速率 | B. | 升高温度可减小反应速率 | ||
| C. | 达到平衡时,v(正)=v(逆)=0 | D. | 达到平衡时,NO2转化率为100% |
12.氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等.某化学兴趣小组用模拟制备氨基
甲酸铵,反应的化学方程式如下:2NH3(g)+CO2(g)?NH2COONH4(s)△H<0
(1)如用如图1装置制取氨气,你所选择的试剂是浓氨水与生石灰或氢氧化钠固体等.
(2)制备氨基甲酸铵的装置如图2所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中. 当悬浮物较多时,停止制备.
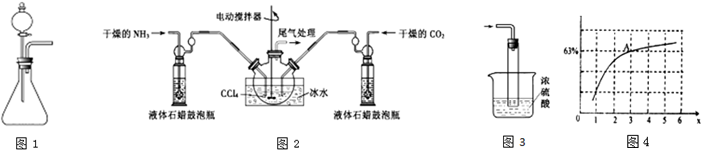
注:四氯化碳与液体石蜡均为惰性介质.
①制备氨基甲酸铵时温度不能高,该实验中控温措施有哪些搅拌、冰水浴、控制通入气体流速.
②从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称).为了得到干燥产品,应采取的方法是c(填写选项序号).
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
③尾气处理装置如右图所示.双通玻璃管的作用:防止倒吸;浓硫酸的作用:吸收多余氨气、防止空气中水蒸气进入反应器使氨基甲酸铵水解
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.782 0g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g.则样品中氨基甲酸铵的物质的量分数为80.00%.
[Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(CaCO3)=100]
(4)以NH3和CO2为原料在工业上生产尿素的原理是:2NH3(g)+CO2(g)?CO(NH2)(I)+H2O(I),该反应的平衡常数和温度关系如下:
①焓变△H<0(填“>”、“<”或“=”).
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比),
如图4是氨碳比(x),$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=x与CO2平衡转化率(a)的关系.
a随着x增大而增大的原因是NH3的量增大,平衡正向移动,则增大CO2的转化率.,图中A点处NH3的平衡转化率为42%.
甲酸铵,反应的化学方程式如下:2NH3(g)+CO2(g)?NH2COONH4(s)△H<0
(1)如用如图1装置制取氨气,你所选择的试剂是浓氨水与生石灰或氢氧化钠固体等.
(2)制备氨基甲酸铵的装置如图2所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中. 当悬浮物较多时,停止制备.

注:四氯化碳与液体石蜡均为惰性介质.
①制备氨基甲酸铵时温度不能高,该实验中控温措施有哪些搅拌、冰水浴、控制通入气体流速.
②从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称).为了得到干燥产品,应采取的方法是c(填写选项序号).
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
③尾气处理装置如右图所示.双通玻璃管的作用:防止倒吸;浓硫酸的作用:吸收多余氨气、防止空气中水蒸气进入反应器使氨基甲酸铵水解
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.782 0g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g.则样品中氨基甲酸铵的物质的量分数为80.00%.
[Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(CaCO3)=100]
(4)以NH3和CO2为原料在工业上生产尿素的原理是:2NH3(g)+CO2(g)?CO(NH2)(I)+H2O(I),该反应的平衡常数和温度关系如下:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比),
如图4是氨碳比(x),$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=x与CO2平衡转化率(a)的关系.
a随着x增大而增大的原因是NH3的量增大,平衡正向移动,则增大CO2的转化率.,图中A点处NH3的平衡转化率为42%.
