��Ŀ����
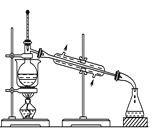
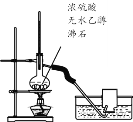
����Ŀ����1��ʵ������ȡ��Ȳ�Ļ�ѧ����ʽΪ_________________,���������Ȳʱ��Ҫ��________��Һ���ѧʽ������_________��Һ��ȥ��������H2S��PH3��ʵ������ȡ��ϩ�������ʱ������ˮ�����Ը�����ؼ�����ϩʱ����Ҫ��ȥ________��д��ѧʽ����ͬ���ĸ��ţ������鷢����ȥ��Ӧʱ�����Ը��������Һ�������ʱ�Ƿ���Ҫ���ӣ������ԭ��_________________________________________��
��2��������¹����γɵķ�ɢϵ���з��ࣺ�ٻ����ͼ��뵽ˮ�к��ֽ��裻��������ˮ�м����������ǡ�ñ��ͣ��۱����Ȼ�����Һ����μ�����������������Һ��������������Һ��ͨ�������CO2��������ֽ�����������������õ�����Һ�� �����ײ��Ϸ�ɢ���������Ʊ����ϲ��ϣ��ߵ�ˮ�;ƾ��Ļ������ڽ������____________��һ��ͨ��_______________��������塣
��3��ȡ2.08gijNaHSO3��Ħ������Ϊ104g/mol����Ʒ������ˮ����ת�Ƶ�100mL����ƿ�У�������ˮ���ݣ�ȡ��5mL������0.01mol/L KMnO4������Һ�ζ�������ΪMn2+������ȥ10.00mL��д���ζ������з�����Ӧ�����ӷ���ʽ____________������Ʒ�Ĵ���Ϊ_______
��4��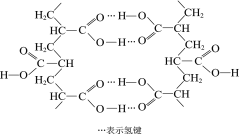 ������Ľṹ��ʽΪ__________________
������Ľṹ��ʽΪ__________________
���𰸡�CaC2 +2 H2O![]() Ca(OH)2 +
Ca(OH)2 +![]() �� Br2������KMnO4 ����ͭ SO2 ��Ҫ���ӣ�ԭ�����������������ƴ���Һ�з�����ȥ��Ӧ����ϩ���������Ҵ������߶�Ҫ�����Ը��������Һ����������ԭ��Ӧ�� �ݢ� �����
�� Br2������KMnO4 ����ͭ SO2 ��Ҫ���ӣ�ԭ�����������������ƴ���Һ�з�����ȥ��Ӧ����ϩ���������Ҵ������߶�Ҫ�����Ը��������Һ����������ԭ��Ӧ�� �ݢ� ����� ![]() 25% CH2=CHCOOH
25% CH2=CHCOOH
��������
��ʵ������ȡ��Ȳ�Ļ�ѧ����ʽΪCaC2 +2 H2O![]() Ca(OH)2 +
Ca(OH)2 +![]() �������������Ȳʱ��Ҫ����ˮ�����Ը��������Һ��������ͭ��Һ��ȥ��������H2S��PH3��ʵ������ȡ��ϩ�������ʱ������ˮ�����Ը�����ؼ�����ϩʱ����Ҫ��ȥSO2�ĸ��ţ������鷢����ȥ��Ӧʱ�����Ը��������Һ�������ʱ��Ҫ���ӣ�ԭ�����������������ƴ���Һ�з�����ȥ��Ӧ����ϩ���������Ҵ������߶�Ҫ�����Ը��������Һ����������ԭ��Ӧ��
�������������Ȳʱ��Ҫ����ˮ�����Ը��������Һ��������ͭ��Һ��ȥ��������H2S��PH3��ʵ������ȡ��ϩ�������ʱ������ˮ�����Ը�����ؼ�����ϩʱ����Ҫ��ȥSO2�ĸ��ţ������鷢����ȥ��Ӧʱ�����Ը��������Һ�������ʱ��Ҫ���ӣ�ԭ�����������������ƴ���Һ�з�����ȥ��Ӧ����ϩ���������Ҵ������߶�Ҫ�����Ը��������Һ����������ԭ��Ӧ��
�ʴ�Ϊ��CaC2 +2 H2O![]() Ca(OH)2 +
Ca(OH)2 +![]() ����Br2������KMnO4������ͭ��SO2����Ҫ���ӣ�ԭ�����������������ƴ���Һ�з�����ȥ��Ӧ����ϩ���������Ҵ������߶�Ҫ�����Ը��������Һ����������ԭ��Ӧ��
����Br2������KMnO4������ͭ��SO2����Ҫ���ӣ�ԭ�����������������ƴ���Һ�з�����ȥ��Ӧ����ϩ���������Ҵ������߶�Ҫ�����Ը��������Һ����������ԭ��Ӧ��
�Ƣٻ����ͼ��뵽ˮ�к��ֽ��裬�γ�����Һ�����ú����߷ֲ㲻���ܣ�
��������ˮ�м����������ǡ�ñ��ͣ��γ���Һ��
�۱����Ȼ�����Һ����μ�����������������Һ���γɳ�����
������������Һ��ͨ�������CO2���γɳ������������ܽ��Ϊ��Һ��
������ֽ�����������������õ�����Һ�����������ֽ����Ȼ�ǽ��壻
�����ײ��Ϸ�ɢ���������Ʊ����ϲ��ϣ����Ͻ������������ڽ��壻
�ߵ�ˮ�;ƾ��Ļ�������Һ��
���ڽ�����Ǣݢޣ�һ��ͨ���������������塣
�ʴ�Ϊ���ݢޣ��������
��NaHSO3��KMnO4������Һ��Ӧ��KMnO4����ԭΪMn2+����HSO3-������ΪSO42-��������Ӧ�����ӷ���ʽΪ![]() ��
��
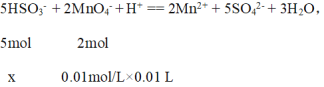
����õ�x = 2.5��10-4 mol��
����Ʒ�Ĵ���Ϊ![]() ��
��
�ʴ�Ϊ��![]() ��25%��
��25%��
�� ��ͨ������������Ľṹ��ʽΪCH2=CHCOOH��
��ͨ������������Ľṹ��ʽΪCH2=CHCOOH��
�ʴ�ΪCH2=CHCOOH��