题目内容
【题目】某温度时,两个恒容密闭容器中仅发生反应2NO2(g)![]() 2NO(g) +O2(g) ΔH > 0。实验测得:υ正(NO2)=k正c2(NO2),υ逆(NO)=k逆c2(NO)·c(O2),k正、k逆为化学反应速率常数,只受温度影响。
2NO(g) +O2(g) ΔH > 0。实验测得:υ正(NO2)=k正c2(NO2),υ逆(NO)=k逆c2(NO)·c(O2),k正、k逆为化学反应速率常数,只受温度影响。
容器 编号 | 起始浓度(mol·L1) | 平衡浓度(mol·L1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.6 | 0.1 | 0 | |
下列说法不正确的是
A.Ⅰ中NO2的平衡转化率约为66.7%
B.Ⅱ中达到平衡状态时,c(O2)<0.2 mol·L1
C.该反应的化学平衡常数可表示为K=![]()
D.升高温度,该反应的化学平衡常数减小
【答案】D
【解析】
先用三段式法计算出实验Ⅰ中各组分的改变浓度和平衡浓度:

而实验Ⅱ相当于在Ⅰ基础上再加入NO,平衡会逆向移动,再判断各量的变化。
A、由上述分析可知,Ⅰ中NO2的平衡转化率为![]() ,故A正确;
,故A正确;
B、Ⅰ中平衡时c(O2)=0.2 mol·L1,实验Ⅱ相当于在Ⅰ基础上再加入NO,平衡会逆向移动,c(O2)<0.2 mol·L1,故B正确;
C、平衡时υ正(NO2)=υ逆(NO),即k正c2(NO2)=k逆c2(NO)·c(O2),得![]() =
=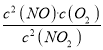 =K,故C正确;
=K,故C正确;
D、该反应为吸热反应,升高温度,K值增大,故D错误。
答案选D。

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目