题目内容
12.C1O2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得C1O2:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;加热\;}}{\;}$2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法中正确的是( )
| A. | KClO3在反应中是氧化剂 | |
| B. | 1mol KClO3参加反应,在标准状况下能得到22.4L气体 | |
| C. | 在反应中H2C2O4既不是氧化剂也不是还原剂 | |
| D. | 1mol KClO3参加反应有1mol电子转移 |
分析 2KClO3+H2C2O4+H2SO4$\frac{\underline{\;加热\;}}{\;}$2ClO2↑+K2SO4+2CO2↑+2H2O中,Cl元素的化合价由+5价降低为+4价,C元素的化合价由+3价升高为+4价,以此来解答.
解答 解:A、Cl元素的化合价降低,则KClO3在反应中被还原,故A正确;
B、1mol KClO3参加反应,在标准状况下能得到1molClO2气体和1mol二氧化碳气体,即得到2mol气体,其体积为44.8L,故B错误;
C、化合价升高元素是C元素所在的反应物H2C2O4是还原剂,故C错误;
D、根据化学方程式,2molKClO3参加反应有2mol电子转移,所以1molKClO3参加反应有1mol电子转移,故D正确;
故选AD.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重基本概念和电子转移的考查,题目难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
3.已知可逆反应温度为T0时,在容积固定的密闭容器中发生 X(g)+Y(g)?Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a 所示.其他条件相同,温度分别为 T1、T2时发生反应;Z 的浓度随时间变化的关系如图b 所示.下列叙述正确的是( )
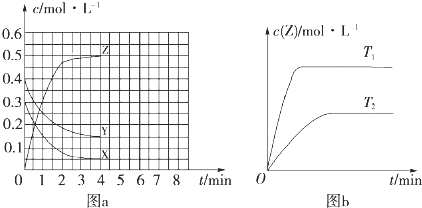

| A. | 发生反应时,各物质的反应速率大小关系为v(X)=v (Y)=2 v (Z) | |
| B. | 图a 中反应达到平衡时,Y 的转化率为37.5% | |
| C. | T0 时,该反应的平衡常数为 33.3 | |
| D. | 该反应正反应的反应热△H<0 |
20.下列说法正确的是( )
| A. | 27gAl与足量浓硫酸混合,产生气体33.6L(标况) | |
| B. | 1molSiO2与C完全反应,生成标准状况气体44.8L | |
| C. | 电解精炼Cu时,阳极每溶解12.8gCu,阴极析出0.2molCu | |
| D. | 1mol/L的某一元酸溶液,测得pH=3,溶液中c(OH-)一定为1×10-11 |
17.常温下,一元酸HA溶液和NaOH溶液等体积混合(忽略体积变化),实验数据如下表下列判断正确的是( )
| 实验编号 | 起始浓度/mol•L-1 | 反应后溶液的pH | |
| c(HA) | c(NaOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | X | 0.2 | 7 |
| ③ | 0.2 | 0.1 | 4.8 |
| ④ | 0.1 | 0.2 | y |
| A. | 实验①反应后的溶液中:c(HA)约为$\frac{{K}_{W}}{1×1{0}^{-9}}$mol•L-1 | |
| B. | 实验②反应后的溶液中:c(HA)>c(Na+)=c(A-)>c(H+)=c(OH-) | |
| C. | 实验③反应后的溶液中:c(HA)+c(H+)=c(OH-)+c(A-) | |
| D. | 实验④反应后的溶液中:c(OH-)-c(H+)-c(HA)=0.05mol•L-1 |
4.下列操作能促进水的电离,且使溶液的pH>7的是( )
| A. | 将纯水加热到90℃ | B. | 向水中加少量Na2CO3溶液 | ||
| C. | 向水中加少量NaOH溶液 | D. | 向水中加少量FeCl3溶液 |
1.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下一定呈气态 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 化合物AE与CE有相同类型的化学键 |
19.1999年曾报道合成和分离了含高能量的N5+的化合物N5AsF6,下列叙述错误的是( )
| A. | N5+中氮-氮之间是以共价键结合 | B. | N5+具有35个电子 | ||
| C. | 化合物N5AsF6中As的化合价为+5 | D. | 化合物N5AsF6中F的化合价为-1 |
 .
. .
. (写出结构简式).
(写出结构简式).