题目内容
4.下列操作能促进水的电离,且使溶液的pH>7的是( )| A. | 将纯水加热到90℃ | B. | 向水中加少量Na2CO3溶液 | ||
| C. | 向水中加少量NaOH溶液 | D. | 向水中加少量FeCl3溶液 |
分析 水的电离是吸热反应,升高温度促进水电离,水电离生成氢离子和氢氧根离子,所以酸或碱、强酸酸式盐都抑制水电离,含有弱离子的盐促进水电离,据此分析解答.
解答 解:水的电离是吸热反应,升高温度促进水电离,水电离生成氢离子和氢氧根离子,所以酸或碱、强酸酸式盐都抑制水电离,含有弱离子的盐促进水电离,
A.升高温度促进水电离,溶液中氢离子浓度增大,溶液的pH减小,故A错误;
B.碳酸钠是强碱弱酸盐,碳酸根离子水解促进水电离,生成氢氧根离子而导致溶液呈碱性,故B正确;
C.NaOH电离生成氢氧根离子而抑制水电离,故C错误;
D.氯化铁是强酸弱碱盐,铁离子水解而促进水电离,生成氢离子而导致溶液呈酸性,故D错误;
故选B.
点评 本题以水的电离为载体考查盐类水解、水电离影响因素,侧重考查分析能力,明确水电离特点及盐类水解特点即可解答,注意升高温度促进水电离但溶液不能变为酸性或碱性,为易错点.

练习册系列答案
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
15.断肠草(Gelsemium)为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出的四种毒素的结构式,下列推断正确的是( )


| A. | ①和②、③与④分别互为同分异构体 | |
| B. | ①、③互为同系物 | |
| C. | ①、②、③、④均能与氢氧化钠溶液反应 | |
| D. | 等物质的量的②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者少 |
12.C1O2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得C1O2:
2KClO3+H2C2O4+H2SO4$\frac{\underline{\;加热\;}}{\;}$2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法中正确的是( )
2KClO3+H2C2O4+H2SO4$\frac{\underline{\;加热\;}}{\;}$2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法中正确的是( )
| A. | KClO3在反应中是氧化剂 | |
| B. | 1mol KClO3参加反应,在标准状况下能得到22.4L气体 | |
| C. | 在反应中H2C2O4既不是氧化剂也不是还原剂 | |
| D. | 1mol KClO3参加反应有1mol电子转移 |
9.常温下,下图是用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/LHA溶液所得到滴定曲线.下列相关的说法错误的是(忽略滴定前后体积变化)( )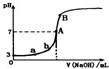

| A. | 由图可知HA是一种弱酸,且Ka=1.0×10-5 | |
| B. | 水电离出的氢离子浓度:a<b | |
| C. | 当NaOH溶液的体积为10.00mL时,有:c(A-)+c(OH-)=c(H+)+c(HA) | |
| D. | B点溶液中的离子浓度关系为:c(Na+)>c(A-)>c(OH-)>c(H+) |
16.向某无色溶液中加入铝片能放出氢气,则此溶液中一定能大量共存的离子组是( )
| A. | Ba2+、Cl-、Na+、K+ | B. | K+、Na+、NO3-、HCO3- | ||
| C. | Na+、SO32-、Cl-、NO3- | D. | Fe3+、Na+、AlO2-、SO42- |
11.有机化合物A的分子式为C5H12O,且能与金属钠反应放出氢气,那么A的同分异构体的数目(包括A)为( )
| A. | 8种 | B. | 7种 | C. | 6种 | D. | 5种 |
 2NH3(g)△H=-92.4kJ·mol-1,开始他们将N2和H2混合气体20mol(体积比1:1)充入5L合成塔中。反应前压强为P。,反应过程中压强用P表示,反应过程中P/P。与时间t的关系如下图所示。请回答下列问题:
2NH3(g)△H=-92.4kJ·mol-1,开始他们将N2和H2混合气体20mol(体积比1:1)充入5L合成塔中。反应前压强为P。,反应过程中压强用P表示,反应过程中P/P。与时间t的关系如下图所示。请回答下列问题:

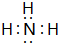 ;B的水溶液不呈中性的原因NH4++H2O?NH3.H2O+H+(用离子方程式表示)
;B的水溶液不呈中性的原因NH4++H2O?NH3.H2O+H+(用离子方程式表示)