题目内容
下表是元素周期表的一部分,回答下列问题:
(1)上表中,可用来制作半导体材料的物质的组成元素是 (填元素符号).
(2)S元素的最高正化合价是 .
(3)Na、Mg、Al三种元素的金属性逐渐 (填“减弱”或“增强”).
(4)某元素位于元素周期表中第3周期第ⅦA族,该元素的原子结构示意图是 (选填编号).
a. b.
b. c.
c.
(5)化学键的断裂和形成都伴随着能量变化,那么1mol H2O→2mol H+1mol O的变化过程要 (填“吸收”或“放出”)能量.
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | O | ||||||
| 3 | Na | Mg | Al | Si | S | |||
(2)S元素的最高正化合价是
(3)Na、Mg、Al三种元素的金属性逐渐
(4)某元素位于元素周期表中第3周期第ⅦA族,该元素的原子结构示意图是
a.
 b.
b. c.
c.
(5)化学键的断裂和形成都伴随着能量变化,那么1mol H2O→2mol H+1mol O的变化过程要
考点:元素周期表的结构及其应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)用来制作半导体材料的物质的组成元素为硅;
(2)S元素为第ⅥA元素,最高正价等于族序数;
(3)Na、Mg、Al三种元素位于同周期,原子序数大的金属性弱;
(4)位于元素周期表中第3周期第ⅦA族,则原子结构中有3个电子层,最外层电子数为7;
(5)断裂化学键需要吸收能量.
(2)S元素为第ⅥA元素,最高正价等于族序数;
(3)Na、Mg、Al三种元素位于同周期,原子序数大的金属性弱;
(4)位于元素周期表中第3周期第ⅦA族,则原子结构中有3个电子层,最外层电子数为7;
(5)断裂化学键需要吸收能量.
解答:
解:(1)用来制作半导体材料的物质的组成元素为硅,其组成元素的元素符号Si,故答案为:Si;
(2)S元素为第ⅥA元素,最高正价等于族序数,则最高价为+6价,故答案为:+6;
(3)Na、Mg、Al三种元素位于同周期,原子序数大的金属性弱,则Na、Mg、Al三种元素的金属性逐渐减弱,故答案为:减弱;
(4)位于元素周期表中第3周期第ⅦA族,则原子结构中有3个电子层,最外层电子数为7,只有c符号,故答案为:c;
(5)断裂化学键需要吸收能量,则1mol H2O→2mol H+1mol O的变化过程要吸收能量,故答案为:吸收.
(2)S元素为第ⅥA元素,最高正价等于族序数,则最高价为+6价,故答案为:+6;
(3)Na、Mg、Al三种元素位于同周期,原子序数大的金属性弱,则Na、Mg、Al三种元素的金属性逐渐减弱,故答案为:减弱;
(4)位于元素周期表中第3周期第ⅦA族,则原子结构中有3个电子层,最外层电子数为7,只有c符号,故答案为:c;
(5)断裂化学键需要吸收能量,则1mol H2O→2mol H+1mol O的变化过程要吸收能量,故答案为:吸收.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、元素的性质及原子结构与位置的关系为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
下列化学反应属于加成反应的是( )
| A、油脂的皂化反应 |
| B、苯与浓硝酸、浓硫酸混合反应 |
| C、在一定条件下,苯与氢气的反应 |
| D、乙烯通入溴的四氯化碳溶液中的反应 |
X、Y、Z、M、W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍.Z与其同主族的短周期元素可形成常见气体甲(甲有刺激性气味).X、Y、Z 三种元素形成化合物乙.下列说法不正确的是( )
| A、原子半径:W>Y>Z>M>X |
| B、X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM |
| C、W与Z两元素形成的化合物是原子晶体 |
| D、化合物乙中一定只有共价键 |
下列图示与对应的叙述相符的是( )
A、 图中曲线表示向等体积、等物质的量浓度的盐酸和醋酸溶液中,分别加入足量镁粉,产生H2的物质的量的变化 |
B、 图表示用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由曲线可确定③的酸性最强 |
C、 图为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
D、 图表示将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数时,二者pH的变化 |

 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.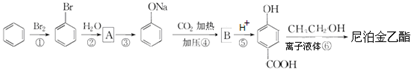
 ⑥
⑥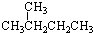 ⑦
⑦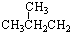 ⑧
⑧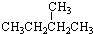
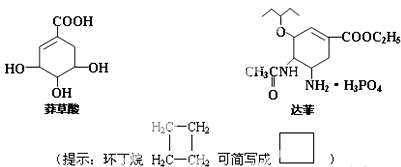
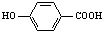 ),其反应类型为:
),其反应类型为: