题目内容
X、Y、Z、M、W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍.Z与其同主族的短周期元素可形成常见气体甲(甲有刺激性气味).X、Y、Z 三种元素形成化合物乙.下列说法不正确的是( )
| A、原子半径:W>Y>Z>M>X |
| B、X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM |
| C、W与Z两元素形成的化合物是原子晶体 |
| D、化合物乙中一定只有共价键 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z、M、W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,则X为H元素;
Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍,而Z与其同主族的短周期元素可形成常见气体甲(甲有刺激性气味),则Z为O元素,可推知Y为N元素、M为F元素、W为Si,故甲为SO2,X、Y、Z 三种元素形成化合物乙为HNO3、NH4NO3等.
Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍,而Z与其同主族的短周期元素可形成常见气体甲(甲有刺激性气味),则Z为O元素,可推知Y为N元素、M为F元素、W为Si,故甲为SO2,X、Y、Z 三种元素形成化合物乙为HNO3、NH4NO3等.
解答:
解:X、Y、Z、M、W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,则X为H元素;
Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍,而Z与其同主族的短周期元素可形成常见气体甲(甲有刺激性气味),则Z为O元素,可推知Y为N元素、M为F元素、W为Si,故甲为SO2,X、Y、Z 三种元素形成化合物乙为HNO3、NH4NO3等,
A.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Si>N>O>F>H,故A正确;
B.非金属性F最强,故氢化物中HF最稳定,常温下水为液态,而HF为气体,故沸点沸点H2O>HF,故B正确;
C.W与Z两元素形成的化合物是二氧化硅,属于原子晶体,故C正确;
D.化合物乙若为NH4NO3,属于离子晶体,含有离子键,故D错误,
故选D.
Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍,而Z与其同主族的短周期元素可形成常见气体甲(甲有刺激性气味),则Z为O元素,可推知Y为N元素、M为F元素、W为Si,故甲为SO2,X、Y、Z 三种元素形成化合物乙为HNO3、NH4NO3等,
A.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Si>N>O>F>H,故A正确;
B.非金属性F最强,故氢化物中HF最稳定,常温下水为液态,而HF为气体,故沸点沸点H2O>HF,故B正确;
C.W与Z两元素形成的化合物是二氧化硅,属于原子晶体,故C正确;
D.化合物乙若为NH4NO3,属于离子晶体,含有离子键,故D错误,
故选D.
点评:本题考查结构性质位置关系应用,难度中等,推断元素是解题关键,注意乙物质的不确定性.

练习册系列答案
相关题目
一定量的铜与100mL一定浓度的硝酸恰好完全反应生成硝酸铜和NO、NO2、N2O4的混合气体,将该混合气体收集在集气瓶中,把集气瓶倒立在水中,通入4.48L的氧气(在标准状况下)可以使集气瓶充满溶液.则下列说法一定正确的是( )
| A、铜的质量为12.8g |
| B、硝酸的物质的量浓度为12mol?L-1 |
| C、体现酸性的硝酸为0.8mol |
| D、被还原的硝酸为0.4mol |
下列说法正确的是( )
| A、胶体均为无色透明的液体 |
| B、不能跟酸反应的氧化物一定能跟碱反应 |
| C、石油分馏、干冰升华、煤的干馏都只涉及物理变化 |
| D、向沸水中逐滴加入少量FeCl3饱和溶液,可制得Fe(OH)3胶体 |
下列说法正确的是( )
| A、氯化钠熔化或氯化氢溶于水时都要破坏化学键 |
| B、常温常压下,18g D2O含有6.02×1024个电子 |
| C、标准状况下,11.2L SO3所含3.01×1023个分子 |
| D、离子化合物中可能含有共价键,共价化合物中一定不含有离子键 |
按如图所示装置进行有关实验,则下列叙述正确的是( )
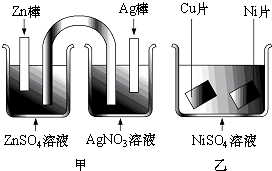

| A、甲装置用作原电池时,锌为正极 |
| B、甲装置用作原电池时,银棒上发生:Ag++e-=Ag |
| C、乙装置用作铜片镀镍时,镍作阴极 |
| D、实现铜片表面镀镍时,可将甲中锌棒与乙中铜片相连,甲中银棒与乙中镍片相连 |
下列化学用语表述正确的是( )
| A、CH3COONH4的电离方程式为:CH3COONH4═CH3COO-+NH4+ | ||||
| B、NaHS的水解方程式为:HS-+H2O═S2-+H3O+ | ||||
| C、次氯酸的结构式为:H-O-Cl | ||||
D、过量Fe粉与Cl2反应的化学方程式为:Fe+Cl2
|
25℃时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L HA酸溶液,溶液pH变化曲线如图所示,仔细观察如图,判断有关说法中不正确的是( )
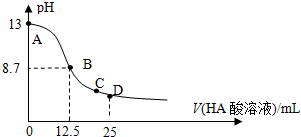

| A、HA酸是弱酸 |
| B、当滴定过程中溶液pH=7时,c(Na+)=c(A-)>c(OH-)=c(H+) |
| C、在C点:c(Na+)>c(A-)>c(H+)>c(OH-) |
| D、在D点:c(A-)+c(HA)=2c(Na+) |
 ;则机理b是
;则机理b是
 b.
b. c.
c.