题目内容
【题目】我国科研工作者研发了电解熔融甲硫醇钠(CH3SNa)制备杀虫剂CH3-S-S-CH3的方法,克服了常规合成法造成的污染,并大幅度提高了原料转化率。基本原理如图所示,A、B为惰性电极,CH3-S-S-CH3在A电极产生,下列说法错误的是( )
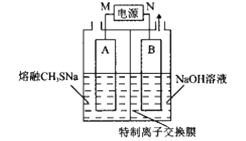
A.M极为电源的正极,B极为电解池的阴极
B.A极的电极反应:2CH3S-+2e-═CH3-S-S-CH3
C.装置中的离子交换膜为阳离子交换膜
D.该装置工作一段时间,右侧电极室中NaOH浓度减小
【答案】BD
【解析】
由电解装置图可知,熔融甲硫醇钠在阳极失电子发生氧化反应生成CH3-S-S-CH3,电极反应为:2CH3S--2e-═CH3-S-S-CH3,则A电极为电解池的阳极,与电源正极相接,所以M极为电源的正极,N极为电源的负极,B极为电解池的阴极,氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑,电解过程中阳极区的钠离子通过离子交换膜移向阴极,据此分析解答。
A.由上述分析可知,M极为电源的正极,B极为电解池的阴极,故A正确;
B.A电极为电解池的阳极,熔融甲硫醇钠失电子发生氧化反应生成CH3-S-S-CH3,电极反应为:2CH3S--2e-═CH3-S-S-CH3,故B错误;
C.电解过程中阳极区的钠离子通过离子交换膜移向阴极,所以装置中的离子交换膜为阳离子交换膜,故C正确;
D.该装置工作一段时间,右侧电极室中氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑,钠离子通过离子交换膜移向阴极,所以NaOH浓度增大,故D错误;
答案选BD。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】利用一种钴矿石(主要成分为 Co2O3,含少量 SiO2及铁、铝、锰、镁、钙等金属元素的氧化物)制取CoC2O42H2O 晶体的工艺流程如下:
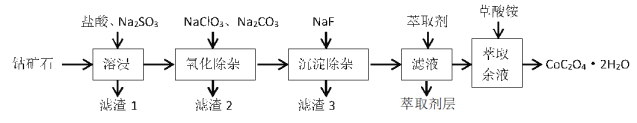
已知部分阳离子以氢氧化物形式沉淀时溶液 pH 如表
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀的 pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)溶浸过程中 Co2O3 发生反应的离子方程式为_____。
(2)氧化除杂过程中加入 Na2CO3 的主要目的是__________,若不加入 NaClO3,其后果是_____。
(3)滤渣 3 的成分是____________,滤液中加入萃取剂的目的是除去_________元素(填元素符号)。
(4)萃取余液中加入草酸铵后,获取 CoC2O4·2H2O 晶体的操作是___________。
(5)含钴化合物 LiCoO2是废旧锂电池的正极材料,可与双氧水、稀 H2SO4 混合加热得到 CoSO4回收利用,该过程发生反应的化学方程式是____________。
(6)已知某温度下 Ksp(MgF2)=7.35×10-11,Ksp(CaF2)=1.05×10-10,当加入过量NaF溶液后,所得滤液中c(Ca2+)/c(Mg2+) =___________。